
下列说法正确的是
A.元素铯的两种核素137Cs比133Cs多四个质子
B.等质量的H2、D2、T2三种气体的电子数之比为2∶3∶6
C.一种元素只能有一种质量数
D.在氮原子中,质子数为7而中子数不一定为7
科目:高中化学 来源:2016届浙江省高一下学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.12C、13C、14C、金刚石、石墨都是碳元素的同位素
B.同种元素的原子,质量数一定相同
C.互为同位素的原子,质子数一定相同
D.由一种元素组成的物质,一定是纯净物
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
在实验室中,常用KMnO4代替MnO2与浓盐酸反应制取氯气,其反应的化学方程式为
2KMnO4+16HCl(浓)= 2MnCl2+5Cl2↑+2KCl+8H2O,下列叙述中正确的是( )
A.反应中KMnO4被氧化
B.氧化产物与还原产物的物质的量之比为2﹕5
C.每生成1 mol Cl2时,反应中转移的电子为2 mol
D.每消耗16 mol HCl时,其中做氧化剂的HCl是10 mol
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:实验题
已知制取氯气也可用浓盐酸与高锰酸钾为原料,其化学方程式为
2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。请回答下列问题:
(1)用双线桥法标出该化学式电子转移的方向与数目:
2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O。
(2)反应中被还原的元素为 (写名称);标准状况下当生成112 L氯气时,反应中转移的电子数目为 。
(3)若有4 molHCl被氧化,则可生成标准状况下的氯气 L。
(4)若有1.58g高锰酸钾和100mL10moL/L浓盐酸充分反应(不考虑盐酸挥发,忽略溶液体积的前后变化),反应至终点时高锰酸钾紫色完全褪去,则被氧化的HCl的物质的量
为 mol。将反应后的溶液取出10mL,加入足量的硝酸银溶液,可得到沉淀的物质的量为 mol。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
某混合气体可能含有N2、HCl和CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体的体积都没有变化。再通过足量的Na2O2固体,气体体积减小。最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。以下对混合气体组成的判断,正确的是
A.一定没有N2,CO和HCl中至少有一种 B.一定有N2、HCl和CO
C.一定有N2 ,CO和HCl中至少有一种 D.一定有N2和HCl,没有CO
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.澄清石灰水跟盐酸反应:OH-+H+=H2O
B.金属钠跟水反应:Na+2H2O=Na++2OH-+H2↑
C.碳酸钡与醋酸反应:BaCO3+2H+=CO2↑+Ba2++H2O
D.碳酸氢钠溶液和氢氧化钠溶液反应:HCO3-+OH-=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源:2016届浙江省湖州市高一上学期期末考试化学试卷(解析版) 题型:填空题
(4分) 实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下
2KMnO4+16HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
(1)在该反应中,还原剂是 。
(2)若在反应中生成了标况下2.24L氯气,则电子转移的个数是 NA。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省湖州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关化学用语表述正确的是
A.质量数为16的氧原子: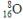
B.漂白粉的有效成分:NaClO
C.Mg2+结构示意图: 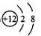
D.钠在氧气中燃烧的化学方程式:4Na+O2  2Na2O
2Na2O
查看答案和解析>>
科目:高中化学 来源:2016届浙江省杭州市高一上学期期末模拟考试化学试卷(解析版) 题型:选择题
下列有关实验的操作、原理和现象,不正确的是( )
A.纸上层析法通常以滤纸作为惰性支持物。滤纸纤维上的羟基具有亲水性,它所吸附的水作固定相
B.重结晶时,溶质的溶解度越大、溶液冷却速度越慢,得到的晶体颗粒越大
C.往海带灰的浸泡液中加入过量的氯水,以保证I-完全氧化为I2
D.将3~4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com