将11.2L(标准状况)乙烯和乙烷的混合气体通入足量溴的四氯化碳溶液中,经充分反应后,溴的四氯化碳溶液增重2.8g.原混合气体中乙烯的体积分数是________;乙烯和乙烷的质量比是________.
20% 7:30
分析:乙烯与溴发生加成反应,根据溴的四氯化碳溶液的质量增加的值,可知乙烯的质量,进而计算乙烯的物质的量,根据气体的总体积可计算混合气体的总物质的量,根据乙烯的物质的量可计算出乙烷的物质的量,根据m=nM计算乙烷的质量,进而计算乙烯的体积分数、二者的质量之比,据此解答.
解答:乙烯与溴发生加成反应,溴的四氯化碳溶液的质量增加了2.8g,
则:m(C
2H
4)=2.8g,
n(C
2H
4)=
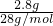
=0.1mol,
又n(C
2H
4)+n(C
2H
6)=
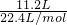
=0.5mol,
则n(C
2H
6)=0.5mol-0.1mol=0.4mol,
故原混合气体中乙烯的体积分数=
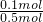
×100%=20%,
m(C
2H
4):n(C
2H
6)=2.8g:0.4mol×30g/mol=7:30,
故答案为:20%;7:30.
点评:本题考查混合物的计算,题目难度不大,注意烯烃与烷烃性质的不同.

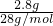 =0.1mol,
=0.1mol,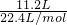 =0.5mol,
=0.5mol,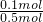 ×100%=20%,
×100%=20%,