
| A、为提高高锰酸钾的氧化能力,用盐酸酸化 | B、为确认某溶液中含有SO42-时,用盐酸酸化,再检验 | C、为检验某氯代烷烃中含氯,加碱溶液加热后用稀硫酸酸化,再检验 | D、为抑制Fe2+ 的水解,用稀硝酸酸化 |


科目:高中化学 来源: 题型:
| A、标准状况下,224mL水含有的电子数为0.1NA | B、1L O.1mol/L硅酸钠溶液中含有O.1NA个SiO32- | C、足量的铁粉与1mol Cl2在加热条件下充分反应,转移的电子数为3NA | D、标准状况下,11.2L C02和S02混合气体中含NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 氢氟酸具有酸性 | 氢氟酸可用于雕刻玻璃 |
| B | SO2有氧化性 | SO2可用于漂白纸浆 |
| C | NH3极易溶于水 | NH3可用作制冷剂 |
| D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2具有漂白性,可用作熏蒸粉丝使其增白 | B、常温下,二氧化硅不与强酸反应,可用石英容器盛放氢氟酸 | C、铜的金属活泼性比铁弱,可在铁船闸上装若干铜块以减缓其腐蚀 | D、氧化铝熔点很高,可制造高温耐火材料,如制耐火管,坩埚等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 污染 | 白色污染 | PM | 氮氧化物 | 水体富营养化 |
| 来源 | 废弃塑料 | 化石燃料燃烧 | 汽车尾气 | 石油化工废弃物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子交换膜在工业生产中广泛应用,如氯碱工业使用了阴离子交换膜 | B、甲醛与尿素反应得到的脲醛树脂是一种高分子黏合剂,广泛应用于木材加工业,是居室甲醛污染的主要来源 | C、目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | D、温室效应导致海水的酸度增加,珊瑚、贝壳类等生物的生存将会受到威胁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
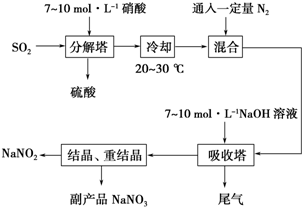
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com