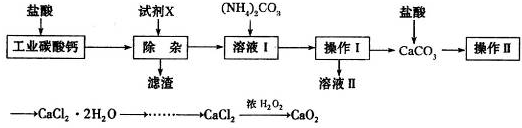
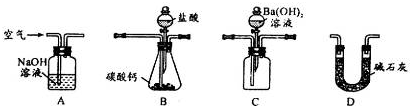
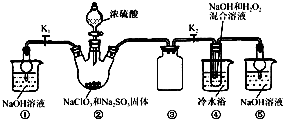
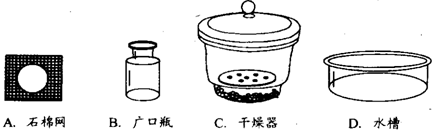
(2013?湖州二模)水合肼是一种重要的精细化工原料,纯品为无色透明的油状液体,在高温下分解成N
2、NH
3和H
2.水合肼具有还原性,能与碘反应:N
2H
4+2I
2═N
2+4HI.在农药、医药及有机合成中有广泛用途.用尿素法制备水合肼,可分为两个阶段,第一阶段为低温氯化阶段,第二阶段为高温水解阶段,总反应方程式为:(NH
2)
2CO+NaClO+2NaOH→N
2H
4?H
2O+NaCl+Na
2CO
3实验步骤:
步骤1.向30%的NaOH溶液中通入Cl
2,保持温度在30℃以下,至溶液显浅黄绿色停止通Cl
2.静置,检测NaClO的浓度后,倾出上层清液,配制所需浓度的NaClO和NaOH的混合溶液.
步骤2.称取一定质量尿素配成溶液,置于冰水浴.将一定体积步骤1配得的溶液倒入分液漏斗中,慢慢滴加到尿素溶液中,0.5h左右滴完后,继续搅拌0.5h.
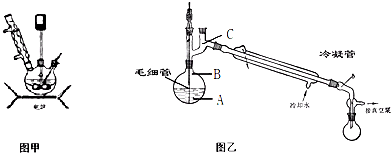
步骤3.将步骤2所得溶液,转移到三口烧瓶(见图甲)并加入5gKMnO
4作催化剂,边搅拌边急速升温,在108℃回流5min.
(1)步骤1中检测NaClO浓度的目的是
确定所需尿素与NaOH的用量
确定所需尿素与NaOH的用量
.步骤2中冰水浴的作用是
减少副反应的发生
减少副反应的发生
.
(2)粗产品倒入图乙的烧瓶中进行减压蒸馏.减压蒸馏的原理是
通过减小体系压强,可以使液体在较低温度下沸腾
通过减小体系压强,可以使液体在较低温度下沸腾
.在烧瓶中插入一根毛细管,通过蒸馏即可得到纯品.在减压蒸馏过程中毛细管的作用是
防止暴沸
防止暴沸
,温度计水银球放置的位置是
C
C
(填写图中A、B、C).
(3)测定水合肼的质量分数可采用下列步骤:
a.准确称取1.250g试样,经溶解、转移、定容等步骤,配制250mL溶液.
b.移取10.00mL于锥形瓶中,加入20mL水,摇匀.
c.用0.1000mol?L
-1碘的标准溶液滴定至溶液出现微黄色且0.5min内不消失,记录消耗溶液的体积.
d.进一步操作与数据处理
①使用容量瓶前要先检漏并洗净,检漏的操作方法是
在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验
在容量瓶中注入适量水,塞上瓶塞,食指顶住瓶塞,另一只手托住瓶底,倒立过来,观察是否漏水,若不漏水,将瓶正立并将瓶塞旋转180°后,再次检验
.
②滴定时,碘的标准溶液盛放在
酸式
酸式
滴定管中(填“酸式”或“碱式”);称取1.250g试样时所用的仪器是
电子天平
电子天平
.
③若本次滴定消耗碘的标准溶液为18.00mL,则产品中N
2H
4?H
2O的质量分数为
90%
90%
.
④为获得更精确的滴定结果,步骤d中进一步的操作是
重复步骤b和c1~2次
重复步骤b和c1~2次
.

 名校课堂系列答案
名校课堂系列答案