
| A. | 铝的金属性比镓强,铝的熔点比镓低 | |
| B. | 铝表面形成致密的氧化膜,所以可以用铝制容器来腌制咸菜 | |
| C. | Ga(OH)3与Al(OH)3性质相似,一定能与NaOH溶液反应 | |
| D. | 铝镓合金与水反应后的物质可以回收利用冶炼铝 |
分析 A、根据同主族元素金属性的递变规律分析,同主族元素从上到下金属性逐渐增强;二者都是金属晶体,金属键越强,熔点越高,二者离子电荷相同,离子半径越大金属键越弱;
B、氯离子会破坏铝表面氧化膜;
C、Ga的金属性比Al强,Ga(OH)3可能不表现为两性氢氧化物;
D、铝镓合金与水反应,铝生成氧化铝,工业上电解熔融的氧化铝冶炼铝.
解答 解:A、同主族元素从上到下金属性逐渐增强,金属性Ge>Al,二者都是金属晶体,离子半径Ge3+>Al3+,故金属Al中的金属键更强,故熔点Al>Ge,故A错误;
B、氯离子会破坏铝表面氧化膜,则不能用铝制容器来腌制咸菜等,故B错误;
C、Ga的金属性比Al强,Ga(OH)3可能不表现为两性氢氧化物,故Ga(OH)3不一定与能与NaOH溶液反应,故C错误;
D、铝镓合金与水反应,铝生成氧化铝,可以回收氧化铝冶炼铝,故D正确;
故选D.
点评 本题考查同族性质的相似性与递变性,难度不大,注意基础知识的积累.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
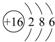
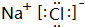 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固态Na2O2和熔融态NaHSO4中的阴、阳离子个数比均为1:1 | |
| B. | 离子化合物中一定不含共价键 | |
| C. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H8-2m+nR或RH8-2m+n | |
| D. | 元素周期表中L层电子为奇数的元素的化合价也都是奇数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲基的电子式 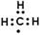 | |
| B. | 乙醛的结构简式为CH3COH | |
| C. | 按系统命名法,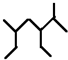 的名称为2,5-二甲基-3-乙基庚烷 的名称为2,5-二甲基-3-乙基庚烷 | |
| D. | 邻甲基苯酚的结构简式为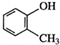 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式:[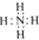 ]+Br- ]+Br- | |
| B. | S2-的结构示意图: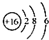 | |
| C. | 原子核内有18个中子的氯分子:${\;}_{17}^{35}$Cl2 | |
| D. | 水分子的形成过程用电子式表示为:H2+ → → |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
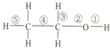 已知乙醇中不同的化学键如图,关于乙醇在各种不同反应中断裂的键的说明不正确的是( )
已知乙醇中不同的化学键如图,关于乙醇在各种不同反应中断裂的键的说明不正确的是( )| A. | 和浓H2SO4共热,140℃时键①②断裂 | B. | 在Ag催化下和O2反应键①③断裂 | ||
| C. | 和浓H2SO4共热,170℃时②⑤键断裂 | D. | 和氢溴反应键①断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m:n之比为2:3 | B. | 18Om和16On的物质的量比为1:1 | ||
| C. | 18Om和16On的质量比为3:4 | D. | 18Om和16On的密度为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液与硫酸的反应 OH-+H+═H2O | |
| B. | 澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 铜片插入硝酸银溶液中 Cu+Ag+═Cu2++Ag | |
| D. | 碳酸钙溶于稀盐酸中 CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com