
右图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggycene”,下列有关doggycene的说法正确的是( )
A.“doggycene”中所有碳原子不可能处于同一平面上
B.该物质的分子式为C26H30
C.常温下该有机物为气态
D.1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为2∶1
科目:高中化学 来源: 题型:
污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
请回答下列问题:

(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、 、 ;其中玻璃棒的作用是 。
(2)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是 。
(3)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀 (此时溶液中c(Ni2+)=1.0×10-5mol/L),溶液中Cu2+的浓度是 。mol/L
(4)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式 。
(5)下列各组试剂中,能准确测定一定体积燃煤尾气中SO2含量的是__________。(填编号)
a.NaOH溶液、酚酞试液
b.稀H2SO4酸化的KMnO4溶液
c.碘水、淀粉溶液
d.氨水、酚酞试液
(6)除杂后得到的MnSO4溶液可以通过 (填操作名称)制得硫酸锰晶体(MnSO4•H2O,相对分子质量为169)。已知废气中SO2浓度为8.4 g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000 m3燃煤尾气,可得硫酸锰晶体质量为 kg (结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是
A.X的氢化物溶于水生成弱酸
B.Z的氢化物的水溶液在空气中存放不易变质
C.Y与X可生成Y3X2型化合物
D.Z的单质在氧气中燃烧可以生成两种酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物在氧气中充分燃烧,生成的水蒸气和二氧化碳的物质的量之比为1∶1,由此可以得出的结论是( )
A.该有机物分子中C、H、O原子个数比为1∶2∶1 B.分子中C、H原子个数比为1∶2
C.该有机物必定含氧 D.可判断该有机物是否含氧
查看答案和解析>>
科目:高中化学 来源: 题型:
松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为加上去的)经下列反应制得:
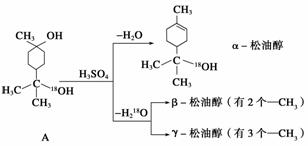
(1)α松油醇的分子式为__________。
(2)α松油醇所属的有机物类别是__________。
a.醇 b.酚 c.饱和一元醇
(3)α松油醇能发生的反应类型是______________。
a.加成 b.水解 c.氧化 d.取代
(4)写出结构简式:β松油醇____________________,γ松油醇
________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH,下列说法正确的是( )
A.浓度均为0.1 mol·L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强
B.0.1 mol·L-1 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小
C.NaF溶液中只含有Na+、F-、H+、OH-、H2O五种微粒
D.NaF溶液中加入少量NaOH固体,溶液中c(F-)变小
查看答案和解析>>
科目:高中化学 来源: 题型:
现有常温下0.1 mol·L-1纯碱溶液。
(1)你认为该溶液呈碱性的原因是(用离子方程式表示)_____________________
___________________________________________________;
为证明你的上述观点,请设计一个简单的实验,简述实验过程:
________________________________________________________________________。
(2)同学甲认为该溶液中Na2CO3的水解是微弱的,发生水解的CO 不超过其总量的10%。请你设计实验证明该同学的观点是否正确:
不超过其总量的10%。请你设计实验证明该同学的观点是否正确:
________________________________________________________________________。
(3)同学乙就该溶液中粒子之间的关系写出了下列四个关系式,你认为其中正确的是( )
A.c(Na+)=2c(CO )
)
B.c(CO )>c(OH-)>c(HCO
)>c(OH-)>c(HCO )>c(H2CO3)
)>c(H2CO3)
C.c(CO )+c(HCO
)+c(HCO )=0.1 mol·L-1
)=0.1 mol·L-1
D.c(OH-)=c(H+)+c(HCO )+2c(H2CO3)
)+2c(H2CO3)
(4)水解反应是典型的可逆反应。水解反应的化学平衡常数称为水解常数(用Kh表示),请写出Na2CO3第一步水解反应的水解常数的表示式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将pH=3的H2SO4和pH=12的NaOH溶液混合,当混合溶液的pH=10时,强酸和强碱的体积之比为( )
A.1∶9 B.9∶1 C.10∶1 D.1∶10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com