
下列反应中,氧化剂与还原剂物质的量之比为1:2的是
A.3S+6NaOH==2Na2S+Na2SO3+3H2O
B.2CH3COOH+Ca(ClO)2==2HClO+Ca(CH3COO)2
C.I2+2NaClO3==2NaIO3+Cl2
D.4HC1(浓)+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:实验题
毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
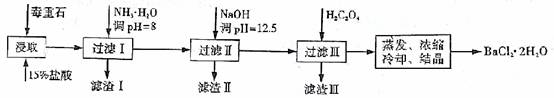
(1)毒重石用盐酸浸取前需充分研磨,目的是 。实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的 。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调节pH=8可除去 (填离子符号),滤渣Ⅱ中含 (填化学式)。加入H2C2O4时应避免过量,原因是 。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H2O;Ba2++CrO42—=BaCrO4↓
步骤Ⅰ:移取xml一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的 (填“上方”或“下方”)。BaCl2溶液的浓度为 mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是
①分子数比为11:16 ②密度比为11:16 ③体积比为16:11 ④原子个数比为11:16
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考二化学卷(解析版) 题型:选择题
在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6g X与Y完全反应后,生成4.4g R,则在此反应中Y和M的质量之比为
A.16:9 B.23:9 C.32:9 D.46:9
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上月考二化学卷(解析版) 题型:选择题
偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生的巨大能量,可作为航天运载火箭的推动力。下列叙述中正确的是
A.偏二甲肼的摩尔质量为60g
B.6.02×1023个偏二甲肼分子的质量为60g
C.1mol偏二甲肼的质量为60g·mol-1
D.6g偏二甲肼含有NA个偏二甲肼分子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:填空题
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法直接排放含SO2的烟气会形成酸雨,危害环境.利用钠碱循环法可脱除烟气中的SO2,在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,
(1)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显________性,用化学平衡原理解释:__________________。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):____________。
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(Na+)>c(HSO3-)>c(SO32-)>c(H-)=c(OH-)
C.c(Na+)+c(H-)=c(SO32-)+c(HSO3-)+c(OH-)
(2) 能证明Na2SO3溶液中存在SO32-+H2O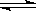 HSO3-+OH-水解平衡的事实是________(填序号)。
HSO3-+OH-水解平衡的事实是________(填序号)。
A.滴入酚酞溶液变红,再加入H2SO4溶液后红色褪去
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
已知Zn(OH)2的溶度积常数为1.2×10-17(mol·L-1)3,则Zn(OH)2在水中的溶解度为
A.1.4×10-6 mol·L-1 B.2.3×10-6 mol·L-1
C.1.4×10-9 mol·L-1 D.2.3×10-9 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
下列有关AgCl沉淀的溶解平衡的说法中,不正确的是
A.AgCl沉淀生成和溶解不断进行,但速率相等
B.AgCl难溶于水 ,溶液中没有Ag+和Cl-
C.升高温度,AgCl沉淀的溶解度增大
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度降低
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆哈密二中高二上期中化学试卷(解析版) 题型:选择题
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:

下列说法中正确的是
A.1molN2(g)和1molO2(g)完全反应放出的能量为180kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com