
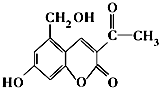
| A. | 亮菌甲素中含有四种官能团 | |
| B. | 亮菌甲素不能与NaHCO3溶液发生反应 | |
| C. | 1 mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2 mol NaOH | |
| D. | 每个亮菌甲素分子在一定条件下与足量H2反应后的产物有3个手性碳原子 |
分析 亮菌甲素中含有醇羟基、酚羟基、碳碳双键、酯基和羰基,所以具有酚、醇、烯烃、酯和酮的性质,能和氢氧化钠反应的官能团是酚羟基、羧基,连有四个不同基团的碳原子形象地称为手性碳原子,以此来解答.
解答 解:A.亮菌甲素含有醇羟基、酚羟基、碳碳双键、酯基和羰基,五种官能团,故A错误;
B.亮菌甲素中含有酚羟基,酸性很弱,不能与NaHCO3溶液发生反应,故B正确;
C.酚-OH、-COOC-及水解生成的酚-OH均与NaOH反应,1mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗3mol NaOH,故C错误;
D.每个亮菌甲素分子在一定条件下与足量H2反应后的产物有6个手性碳原子,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答关键,注意酚、酯、烯烃的性质,侧重分析与应用能力的考查,题目难度不大.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
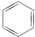 ③(CH3)2C=CH2④
③(CH3)2C=CH2④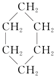 ⑤
⑤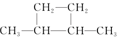
| A. | 链状烃:①③⑤ | B. | 链状烃:③⑤ | C. | 环状烃:②④⑤ | D. | 芳香烃:②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与金属钠反应时,是乙醇分子中羟基中的O-H键断裂 | |
| B. | 检验乙醇中是否含有水,可加入少量无水硫酸铜,若变蓝则含水 | |
| C. | 向待测液中加入饱和碳酸钠溶液鉴别乙酸、乙酸乙酯、乙醇 | |
| D. | 向苯和苯酚混合溶液中滴加过量浓溴水除去混合溶液中的苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾原子的结构示意图为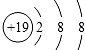 | B. | 水分子的结构式:H-O-H | ||
| C. | NH3的电子式为 | D. | NaOH的电子式为Na+[OH]- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c1:c2=3:1 | |
| B. | 平衡时,Y和Z的生成速率之比为2:3 | |
| C. | X、Y的转化率相等 | |
| D. | c1的取值范围为0 mol/L≤c1≤0.14 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,说明氯水中含有Cl2 | |
| B. | 向FeCl2溶液中滴加氯水,溶液颜色变为棕黄色,说明氯水中含有HClO | |
| C. | 向氯水中滴加稀硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| D. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉与氧化镁共热可制取金属镁 | |
| B. | 铝分别与足量的 HCl溶液、足量的NaOH的溶液反应,产生的氢气前者多 | |
| C. | 可用Na2SiO3溶液和CO2反应来制备H2SiO3 | |
| D. | NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2的消耗量是3.0mol | |
| B. | N2的平均速率是0.5mol•(L•min)-1 | |
| C. | N2的平衡浓度是1.0mol•L-1 | |
| D. | N2反应的量占原物质的量的百分数是50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com