
下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是( )
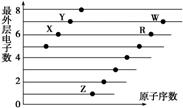
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:Y>X
D.X、Z形成的化合物中可能含有共价键
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组对铝表面氧化膜的保护作用展开了研究,他们查阅有关资料得知:尽管铝表面致密的氧化膜能使铝与其周围的介质(如空气、水等)隔绝,对铝制品起到保护作用,但铝制容器仍不能长期盛放或腌制咸菜。该小组同学设计了一个实验以探究其中的原因。他们的实验过程如下所示:
| 实验 | ||
| 编号 | 实验过程 | 实验现象 |
| 1 | 取一小片铝片于试管中,加入2 mL 1.0 mol·L-1盐酸 | 30 s时开始有少量气泡,然后产生气泡的速率逐渐加快,最后铝片消失 |
| 2 | 取一小片铝片于试管中,加入2 mL 0.5 mol·L-1硫酸 | 55 s时开始有少量气泡,然后产生气泡的速率逐渐加快,最后铝片消失 |
| 3 | 取一小片铝片于试管中,加入氯化铜稀溶液 | 3 min左右表面产生少量气泡,且铝表面析出一些红色固体 |
| 4 | 取一小片铝片于试管中,加入硫酸铜稀溶液 | 一直没有明显的变化 |
(1)你认为实验1、2中盐酸和硫酸的浓度分别为1.0 mol·L-1、0.5 mol·L-1的原因是__________________________________。
(2)根据该实验现象,你认为铝制容器不能长期盛放或腌制咸菜的原因是__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与金属腐蚀有关的说法正确的是( )
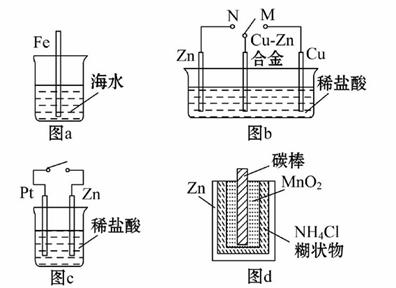
A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时,Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池的放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验装置进行的相应实验,能达到实验目的的是( )
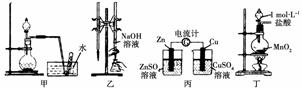
A.用图甲装置进行稀硝酸与铜的反应制取并收集NO
B.用图乙装置进行用已知浓度的氢氧化钠溶液测定盐酸浓度的实验
C.用图丙装置检验电流的方向
D.用图丁装置制取少量Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子或分子在溶液中能大量共存,通入CO2后仍能大量共存的一组是( )
A.K+、Na+、Cl-、NO
B.K+、Na+、Br-、SiO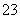
C.H+、Fe2+、SO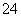 、Cl2
、Cl2
D.K+、Ag+、NH3·H2O、NO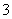
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨水是一种常用的化学试剂。
氨水是一种常用的化学试剂。
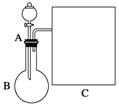
(1)以浓氨水和生石灰为原料,用如右装置为发生装置,可制取少量氨气。已知:NH3·H2O(浓)+CaO===Ca(OH)2+NH3↑。
①生石灰应该装在________(填“A”或“B”)中。
②试从电离平衡角度分析该实验中氨气逸出的原因:_______________。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二:________________。
②请你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、0.25 mol·L-1 NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验 步骤 | 实验操作 | 预期现象 及结论(步骤 1只填现象) |
| 1 | 在A、B两支洁净的试管中各加入1 mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液 | |
| 2 |
(3)取20.00 mL上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.005 0 mol·L-1 的标准硫酸溶液滴定,滴定至锥形瓶溶液出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 mL,则上述氨水的物质的量浓度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于pH=12的Na2CO3溶液说法正确的是( )
A.升高溶液温度,溶液pH增大
B.c(Na+)+c(H+)=c(CO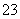 )+c(HCO
)+c(HCO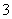 )+c(OH-)
)+c(OH-)
C.溶液中c(OH-)>c(HCO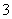 )>c(H+)
)>c(H+)
D.2c(Na+)=c(CO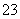 )+c(HCO
)+c(HCO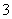 )+c(H2CO3)
)+c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:
Ca(ClO)2+CaCl2+2H2SO4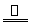 2CaSO4+2Cl2↑+2H2O。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O。他们设计了如下制取氯气并验证其性质的实验。
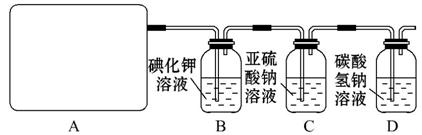
试回答:(1)该实验中A部分的装置是 (填写装置的序号)。
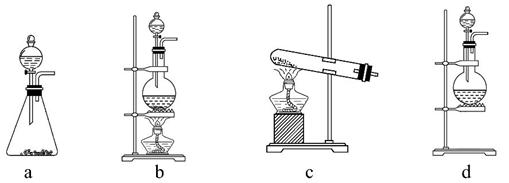
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤): ___________________________________________________________________。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式___________________________________________________________________。
(4)该实验存在明显的缺陷,请你提出改进的方法______________________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 mL溶液,取25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol·L-1的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2====Na2S4O6+ 2NaI反应完成时,共用去Na2S2O320.0 mL。则该漂白粉中Ca(ClO)2的质量分数为: _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关环境保护的说法中错误的是 ( )
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.各国工业大量排放二氧化硫是全球气候变暖的主要原因
C.劣质装修材料中的甲醛、苯、氡气等对人体有害
D.废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com