
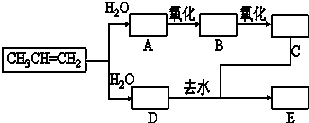
 已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.
已知:①丙烯与水进行加成反应,其可能的产物有两种;②图中E为开链的酯类化合物,其分子式为C6H12O2.分析 丙烯和水发生加成反应生成1-丙醇或2-丙醇,A能连续被氧化,说明A为1-丙醇,其结构简式为CH3CH2CH2OH,1-丙醇为氧化生成B为CH3CH2CHO,丙醛被氧化生成C为CH3CH2COOH,D结构简式为CH3CH(OH)CH3,C和D发生酯化反应生成E,E的分子式为C6H12O2,其结构简式为CH3CH2COOCH(CH3)2,据此分析解答.
解答 解:丙烯和水发生加成反应生成1-丙醇或2-丙醇,A能连续被氧化,说明A为1-丙醇,其结构简式为CH3CH2CH2OH,1-丙醇为氧化生成B为CH3CH2CHO,丙醛被氧化生成C为CH3CH2COOH,D结构简式为CH3CH(OH)CH3,C和D发生酯化反应生成E,E的分子式为C6H12O2,其结构简式为CH3CH2COOCH(CH3)2.
(1)由上述分析可知,A为CH3CH2CH2OH,E为(CH3)2CHOOCCH2CH3,故答案为:CH3CH2CH2OH;(CH3)2CHOOCCH2CH3;
(2)D和浓HBr微热生成有机物F的反应的化学方程式为:CH3CH(OH)CH3+HBr$\stackrel{△}{→}$CH3CHBrCH3+H2O;
D+C→E的方程式:CH3CHOHCH3+CH3CH2COOH$→_{△}^{浓H_{2}SO_{4}}$CH3CH2COOCH(CH3)2+H2O;
B与新制银氨溶液反应的方程式:CH3CH2CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3CH2COONH4+2Ag↓+3NH3↑+H2O,
故答案为:CH3CH(OH)CH3+HBr$\stackrel{△}{→}$CH3CHBrCH3+H2O;CH3CHOHCH3+CH3CH2COOH$→_{△}^{浓H_{2}SO_{4}}$CH3CH2COOCH(CH3)2+H2O;CH3CH2CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3CH2COONH4+2Ag↓+3NH3↑+H2O.
点评 本题考查有机物推断,涉及烯、醇、醛、羧酸、酯之间的转化,明确有机物的官能团及其性质是解本题关键,题目难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
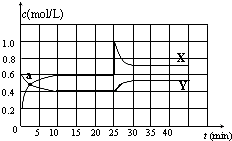 已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )
已知NO2和N2O4可以相互转化:N2O4(g)?2NO2(g)△H<0.在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2L的密闭容器中,反应物浓度随时间变化关系如图.下列说法不正确的是( )| A. | 图中的两条曲线,X是表示NO2浓度随时间的变化曲线 | |
| B. | a点时v(N2O4)=v(NO2) | |
| C. | 25min时改变了影响速率的一个因素,使得NO2转变为N2O4,该改变是将密闭容器的体积缩小,增大压强 | |
| D. | 前10min内用v(N2O4)表示的化学反应速率为0.02 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子层数相同 | B. | 半径大小顺序Na+<Mg2+<Al3+ | ||
| C. | 核外电子数相同 | D. | 最外层电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
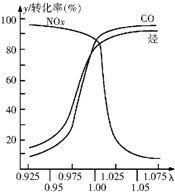 随着经济的发展和生活水平的提高,近年来我省汽车拥有量呈较快增长趋势.
随着经济的发展和生活水平的提高,近年来我省汽车拥有量呈较快增长趋势.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5J•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.
二甲醚(CH3OCH3)是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-23.5J•mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 向NaBr溶液中滴加新制氯水 | 比较Cl2与Br2的氧化性强弱 |
| B | 用同一电路分别测定盐酸和某一元酸溶液的导电性 | 比较盐酸和该一元酸酸性的强弱 |
| C | 分别向AlCl3溶液和MgCl2溶液中加入过量NaOH溶液 | 比较镁与铝的金属性强弱 |
| D | 常温下测定同浓度Na2CO3溶液和Na2SO4溶液的pH值 | 比较硫和碳的非金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +Br2→
+Br2→ ,反应类型是加成反应.
,反应类型是加成反应. .
.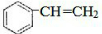 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com