
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
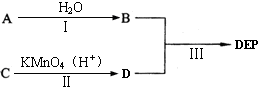 北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).
北京市疾病预防控制中心的调查结果显示,在北京市场上有九成受检香水和三成护发类化妆品被查出致癌物“邻苯二甲酸酯”(PAEs),值得注意的是,在儿童护肤类化妆品中亦有两件样品分别被检出邻苯二甲酸二乙酯(DEP)和邻苯二甲酸二(2-乙基己基)酯(DEHP).
| KMnO4(H+) |
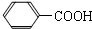
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
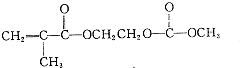
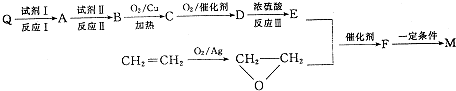
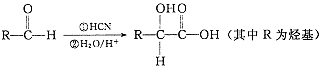
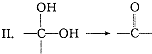
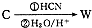 ,请写出符合下列条件的w的一种同分异构体的结构简式
,请写出符合下列条件的w的一种同分异构体的结构简式查看答案和解析>>
科目:高中化学 来源: 题型:
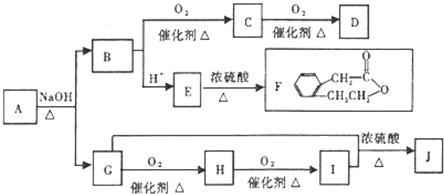
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作过程 | 实验现象 |
| 将干燥的玻璃燃烧匙中燃烧的钠迅速伸入到盛有装满CO2的集气瓶中 | 钠在盛有CO2的集气瓶中继续燃烧 |
| 反应后冷却 | 集气瓶底附着黑色颗粒,瓶壁上附着有白色物质 |
| 实验步骤 | 实验现象 |
| ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 | 出现白色沉淀 |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
| 实验步骤 | 所用试剂及实验操作 |
| ① | 取少量样品放入试管甲中,加入适量蒸馏水并振荡至全部溶解 |
| ② | |
| ③ | 过滤,将少量滤液盛在试管乙中 |
| ④ | 滴入几滴酚酞试液 |
| ⑤ | |
| ⑥ | 向溶液里滴入硝酸银溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com