
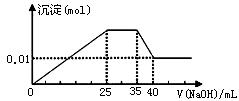
| A.原溶液一定不存在H+、Cu2+、CO32- |
| B.不能确定原溶液是否含有K+、NO3- |
| C.实验所加的NaOH的浓度为2mol·L-1 |
| D.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1:2 |


 考前必练系列答案
考前必练系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.1mol/LCH3COOH溶液的pH>1:CH3COOH?CH3COO-+H+ |
| B.“NO2球”浸泡在冷水中,颜色变浅:2NO2(g)(红棕色)?N2O4(g)(无色)△H<0 |
| C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO═3Fe2++2NO↑+4H2O |
| D.向Na2CO3溶液中滴入酚酞溶液,溶液变红:CO32-+H2O?HCO3-+OH- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 S (n—1)S+ S2-
S (n—1)S+ S2- Sn2-
Sn2-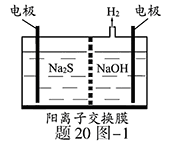
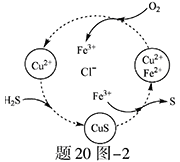
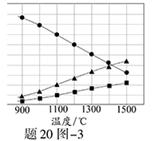
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol·L-1 NaHSO4溶液:K+、Fe2+、NO3-、Cl- |
| B.0.1 mol·L-1NaAlO2的溶液:K+、Na+、SO42-、CO32- |
| C.无色溶液:Ba 2+、Na+、MnO4-、NO3- |
| D.由水电离出的c(OH-)=1.0×10-12 mol·L-1的溶液:NH4+、HCO3-、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg2+、Ca2+、HCO3-、NO3- | B.Al3+、NH4+、Br-、Cl- |
| C.K+、MnO4-、S2-、SO42- | D.Na+、K+、SiO32-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 离子组 | 加入试剂 | 离子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+2NH4++Ba2++2OH-===BaSO4↓+2NH3·H2O |
| B | Mg2+、HCO3-、Cl- | 过量NaOH溶液 | Mg2++2HCO3-+4OH-===2H2O+Mg(OH)2↓+2CO32- |
| C | K+、NH3·H2O、CO32- | 通入少量CO2 | 2OH-+CO2===CO32-+H2O |
| D | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+===SO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Ag+、Br-、MnO4- |
| B.K+、Al3+、AlO2-、SO42- |
| C.Fe3+、H+、I-、SO32- |
| D.Mg2+、NH4+、NO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com