
氧化还原反应中,水可以作氧化剂,作还原剂,既作氧化剂又作还原剂,既不作氧化剂又不作还原剂。下列反应与Br2+SO2+2H2O====H2SO4+2HBr相比较,水的作用不相同的是( )
A.Cl2+H2O HCl+HClO B.2F2+2H2O====4HF+O2
HCl+HClO B.2F2+2H2O====4HF+O2
C.2Na2O2+2H2O====4NaOH+O2↑ D.4Fe(OH)2+O2+2H2O====4Fe(OH)3
科目:高中化学 来源: 题型:
在下列溶液中,各组离子一定能够大量共存的是
A.含SCN-的溶液: Na+、Cl-、SO42-、Fe3+
B.使紫色石蕊试液变蓝的溶液:K+、Ba2+、Cl-、NO3-
C.-使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl-
D.碳酸氢钠溶液:K+、SO42-、Cl-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.Na2O2可用于呼吸面具中氧气的来源
B.Na2O和Na2O2投入水中都能生成NaOH
C.Na2O2和Na2O均可以露置在空气中保存
D.NaCl的性质稳定,可用作调味品
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关离子的检验方法及现象叙述正确的是( )
A.检验H+:向溶液中滴加石蕊试液,溶液变成蓝色,则证明溶液中含有H+
B.检验Cl-:先加入硝酸银溶液,生成白色沉淀,再加入稀硝酸,若沉淀不溶解,则证明含有Cl-
C.检验Fe2+:加入NaOH溶液,产生红褐色沉淀,则证明含有Fe2+
D.检验Fe3+:加入KSCN溶液,生成红色沉淀,则证明含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列递变规律不正确的是 ( )
A.钠、镁、铝单质还原性依次减弱 B.碘、溴、氯单质氧化性依次增强 C.C、N、O原子半径依次减小 D.N、O、F最高正价依次升高
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学小组的同学将一批废弃的线路板简单处理后,得到含Cu、Al、Fe及少量Au、Pt等金属的混合物,并设计了如下制备硫酸铜和硫酸铝晶体的方案:
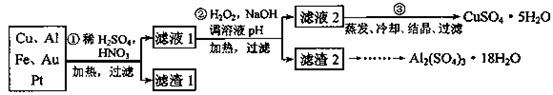
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 2.2 | 3.2 |
| Al3+ | 3.7 | 4.7 |
| Cu 2+ | 5.6 | 6.4 |
回答下列问题:
①第①步参加反应的金属有 。
②第②步加入H2O2是因为滤液1中含有 离子。使用H2O2的优点是 。
③用第③步所得CuSO4·5H2O制备无水硫酸铜的方法是: 。
④请帮助化学小组的同学完成由滤渣2制取Al2(SO4) 3·18H2O 的实验步骤:
(1)取滤渣2,加入足量的 ,充分反应后过滤;
(2)取滤液,加入足量的 (填写试剂的化学式),然后过滤洗涤;
(3)用适量稀硫酸溶解;
(4)最后经过 (填写所需实验操作的名称),获得Al2(SO4)3·18H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于蛋白质的叙述中错误的是
( )
A.蛋白质是两性化合物
B.蛋白质溶液中分别加入浓NaCl溶液、CuSO4溶液,其过程是不可逆的
C.天然蛋白质水解的最终产物是α氨基酸
D.蛋白质分子中的重要化学键是肽键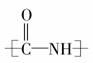
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com