
下列实验操作均用到玻璃棒,其中玻璃棒的作用及其目的相同的是
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
A.①和② B.①和③ C.③和④ D.①和④
科目:高中化学 来源: 题型:阅读理解
 已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:
已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:查看答案和解析>>
科目:高中化学 来源:2011-2012年江苏宿迁泗洪县洪翔中学高二下学期期中考试化学试卷(带解析) 题型:实验题
(10分)已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题: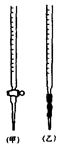
⑴0.0200mol·L-1KMnO4标准溶液应置于 (选填“甲”或“乙”)滴定管中;滴定终点如何判断 。
⑵你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果 ;若回答“否”,试说明原因 。
⑶若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
| A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤 |
| B.滴定前尖嘴部分有一气泡,滴定终点时消失 |
| C.定容时,俯视刻度线 |
| D.滴定前仰视读数,滴定后俯视读数 |
查看答案和解析>>
科目:高中化学 来源:2010年安丘中学高二暑期练习化学卷(四) 题型:实验题
已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化: MnO4-+C2O42-+H+→Mn2++CO2↑+H2O(未配平) MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
⑴配平: MnO4-+ C2O42-+ H+― Mn2++ CO2↑+ H2O
⑵0.0200mol·L-1KMnO4标准溶液应置于 (选填“甲”或“乙”)滴定管中;判断滴定终点的依据是 ;
⑶你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果;若回答“否”,试说明原因 ;
⑷若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
| A.滴定前尖嘴部分有一气泡,滴定终点时消失; | B.溶液转移至容量瓶中,未将烧杯、玻棒洗涤; | C.滴定前仰视读数,滴定后俯视读数; | D.定容时,俯视刻度线;E.锥形瓶水洗之后未用待测液润洗。 |
查看答案和解析>>
科目:高中化学 来源:2011-2012年江苏宿迁泗洪县洪翔中学高二下学期期中考试化学试卷(解析版) 题型:实验题
(10分)已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
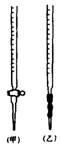
⑴0.0200mol·L-1KMnO4标准溶液应置于 (选填“甲”或“乙”)滴定管中;滴定终点如何判断 。
⑵你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果 ;若回答“否”,试说明原因 。
⑶若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
B.滴定前尖嘴部分有一气泡,滴定终点时消失
C.定容时,俯视刻度线
D.滴定前仰视读数,滴定后俯视读数
E.锥形瓶水洗之后未用待测液润洗
查看答案和解析>>
科目:高中化学 来源:2010年安丘中学高二暑期练习化学卷(四) 题型:实验题
已知KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化: MnO4-+C2O42-+H+→Mn2++CO2↑+H2O(未配平) MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
某研究小组为测定某软锰矿中MnO2的质量分数,准确称取1.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液全部转移到容量瓶中并定容;从中取出25.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,当滴入20.00mLKMnO4溶液时恰好完全反应。试回答下列问题:
⑴配平: MnO4-+ C2O42-+ H+― Mn2++ CO2↑+ H2O
⑵0.0200mol·L-1KMnO4标准溶液应置于 (选填“甲”或“乙”)滴定管中;判断滴定终点的依据是 ;
⑶你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果;若回答“否”,试说明原因 ;
⑷若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.滴定前尖嘴部分有一气泡,滴定终点时消失;B.溶液转移至容量瓶中,未将烧杯、玻棒洗涤;C.滴定前仰视读数,滴定后俯视读数;D.定容时,俯视刻度线;E.锥形瓶水洗之后未用待测液润洗。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com