
在一定条件下,使CO和O2的混合气体26g充分反应,所得混合物在常温下跟足量的Na2O2固体反应,结果固体增重14g,则原混合气体中O2和CO的质量比可能是( )
A. 9:4 B. 1:1 C. 7:6 D. 6:7
考点: 有关混合物反应的计算.
专题: 等量代换法.
分析: 根据2Na2O2+2CO2=2Na2CO3+O2,可知混合物在常温下跟足量的Na2O2固体反应生成固体为Na2CO3,
1molNa2O2生成1molNa2CO3,质量增加28g,恰好为CO的质量,以此判断原混合物中气体的质量之比.
解答: 解:由反应2Na2O2+2CO2=2Na2CO3+O2,可知混合物在常温下跟足量的Na2O2固体反应生成固体为Na2CO3,
1molNa2O2生成1molNa2CO3,质量增加28g,恰好为CO的质量,
固体增重14g,说明混合气体中CO为14g,则O2为26g﹣14g=12g,
所以原混合气体中O2和CO的质量比为12g:14g=6:7,
故选D.
点评: 本题考查混合物的计算,题目难度不大,注意从Na2O2生成Na2CO3质量的变化判断反应的规律,此为解答该题的关键.


科目:高中化学 来源: 题型:
在搪瓷和陶瓷器皿具表面的釉质中含有极微量的Pb、Cd、Sb等有毒金属盐类为防止中毒,不能长期盛放下列物质的是( )
A.食盐 B.酱油 C.蔗糖 D.食醋
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
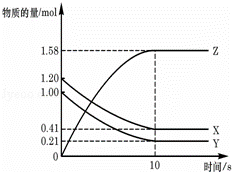
A.反应开始到10s,用Z表示的反应速率为0.158mol/(L•s)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y转化了0.79mol
D.反应的化学方程式为:X(g)+Y(g)⇌Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.0.1 mol·L-1Ba(OH)2溶液中含有0.2NA个OH-
B.1mol Na与足量水反应,转移2NA个电子
C.常温常压下,22.4L乙烯含有NA个CH2=CH2分子
D.常温常压下,46g NO2含有2NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
Fe(OH)3胶体虽然是由FeCl3溶液制得,但两者是截然不同的两种物质.FeCl3溶液、Fe(OH)3胶体共同具备的性质是( )
A. 都呈透明的红褐色
B. 分散质颗粒直径相同
C. 都比较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项操作中,不发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2;
②向NaAlO2溶液中逐滴加入过量的稀盐酸;
③向AlCl3溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硅酸钠溶液中逐滴加入过量的盐酸.
A. ①② B. ①③ C. ①④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合物甲中含有明矾[KAl(SO4)2]、Al2O3和Fe2O3.在一定条件下由甲可实现如图所示的物质之间的转化:
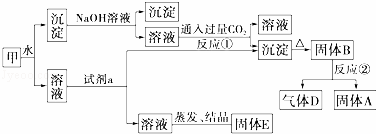
请回答下列问题:
(1)写出A、B、D的化学式:A 、B 、D .
(2)试剂a最好选用 (选填A、B、C、D).
A.NaOH溶液 B.稀盐酸 C.二氧化碳 D.氨水
(3)写出反应①的离子方程式: .
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)⇌SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如右所示.由图可得出的正确结论是( )
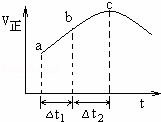
|
| A. | 反应在c点达到平衡状态 |
|
| B. | 反应物浓度:a点小于b点 |
|
| C. | 反应物的总能量低于生成物的总能量 |
|
| D. | △t1=△t2时,SO2的转化率:a~b段小于b~c段 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.MnO2+4HCl MnCl2 +Cl2↑+ 2H2O中,氧化剂和还原剂的物质的量之比为1:4
MnCl2 +Cl2↑+ 2H2O中,氧化剂和还原剂的物质的量之比为1:4
B.2H2S+ SO2==3S+2H2O中,氧化产物和还原产物的质量之比为1:1
C.3S+ 6KOH ==2K2S+ K2SO3+3H2O中,被氧化和被还原的硫元素的物质的量之比为1:1
D.5NH4NO3==4N2↑+2HNO3+9H2O中,发生氧化反应和发生还原反应的氮元素的质量之比为5:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com