
A是一取代芳香化合物,相对分子质量为136,分子中只含碳、氢、氧,其中氧的含量为23.5%。实验表明: A的芳环侧链上只含一个官能团;A和NaOH溶液反应后酸化可以得到E(C7H6O2)和F。
(1)A、E、F的结构简式。
(2)A和NaOH溶液反应、酸化的实验装置如下:
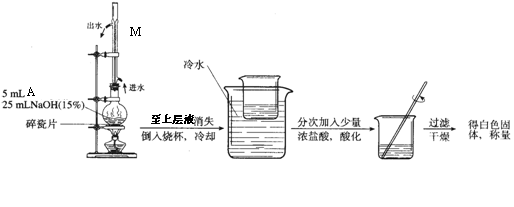

写出A与NaOH溶液反应的化学反应方程式 。
写出实验装置中M的名称和作用 。
(3)A有多种同分异构体,符合下列条件的结构共有 种,
①可以发生银镜反应 ②属于芳香族化合物,不具备其它环状结构
③可以与氢氧化钠溶液反应 ④不能与FeCl3发生显色反应
请写出其中核磁共振氢谱有5个吸收峰的A的结构的结构简式:
【知识点】酯的水解 酯的同分异构体的书写K1 L6
【答案解析】(1)A的结构简式:
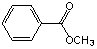 或
或 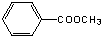
E的结构简式: C6H5COOH ; F的结构简式: CH3OH 。
(2)C6H5COOCH3+NaOH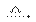 C6H5COONa+CH3OH;冷凝管、冷凝回流。
C6H5COONa+CH3OH;冷凝管、冷凝回流。
(3) 4, 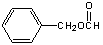
解析:A相对分子质量为136,其中氧的含量为23.5%,所以分子中的氧原子个数为: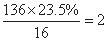 ;结合A是一取代芳香化合物,分子中只含碳、氢、氧,A的芳环侧链上只含一个官能团,即可得到A的结构是:
;结合A是一取代芳香化合物,分子中只含碳、氢、氧,A的芳环侧链上只含一个官能团,即可得到A的结构是: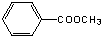 ;A和NaOH溶液反应后酸化可以得到E(C7H6O2)和F,根据酯的水解可知E是苯甲酸:C6H5COOH ,F是甲醇:CH3OH 。
;A和NaOH溶液反应后酸化可以得到E(C7H6O2)和F,根据酯的水解可知E是苯甲酸:C6H5COOH ,F是甲醇:CH3OH 。
(2)根据酯在碱性条件下水解为羧酸盐和醇:C6H5COOCH3+NaOH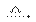 C6H5COONa+CH3OH;装置中M的名称是冷凝管,作用是冷凝回流。
C6H5COONa+CH3OH;装置中M的名称是冷凝管,作用是冷凝回流。
(3)同时符合4个条件的只能是甲酸酯,分别是:
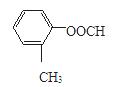
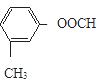
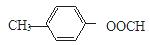 共4种;其中核磁共振氢谱有5个吸收峰的A的结构的结构简式:
共4种;其中核磁共振氢谱有5个吸收峰的A的结构的结构简式: 。
。
【思路点拨】本题考查了酯的水解,及酯的同分异构体的书写,注意理解所给限定条件。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
有关亚硫酸的下列叙述中不正确的是( )
A.亚硫酸是SO2的水溶液,显酸性
B.SO3溶于水,剧烈反应生成亚硫酸
C.亚硫酸具有漂白性,能够使品红溶液褪色
D.亚硫酸不稳定,易分解为水和SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等氧化物杂质)制取金属锌的流程如图所示。
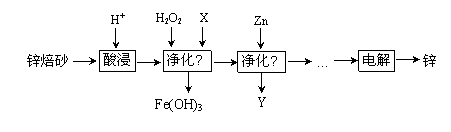

(1)提高酸浸效率的措施为_________________________________(任答一条即可);酸浸时H+与难溶固体ZnFe2O4反应的离子方程式为___________________。
(2)净化Ⅰ中H2O2参与反应的离子方程式为____________________________;X可选择的试剂为______(写化学式)。净化Ⅱ中Y为_____________(写化学式)。
(3)电解法制备锌的装置如图甲所示:
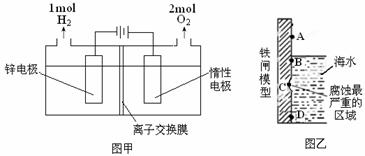
则电解槽中盛有的电解质溶液为______(填字母)。
a.ZnCl2溶液 b.Zn(NO3)2溶液 c.ZnSO4溶液
根据图甲中的数据,可求得电解过程中电流的有效利用率为_________。
(4)使用含有 [Zn(OH)4]2-的强碱性电镀液进行镀锌防腐蚀,可得到细致的光滑镀层,电镀时阴极电极反应式_____________________。以锌为负极,采用牺牲阳极法防止铁闸的腐蚀,图乙中锌块的固定位置最好应在_____处(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
1-对甲苯基-3-苯基-2-丙烯-1-酮(以下用M表示)是一种常见的工业原料,其结构简式为: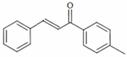 ,工业上合成M线路如下(反应中生成的小分子已略去):
,工业上合成M线路如下(反应中生成的小分子已略去):
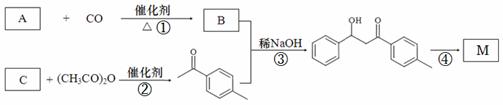
已知:在稀碱作用下,两分子的醛或酮可以互相作用,其中一个醛(或酮)分子中的α-氢加到另一个醛(或酮)分子的羰基氧原子上,其余部分加到羰基碳原子上,生成一分子β-羟基醛或一分子β-羟基酮。
请回答下列问题:
(1)有机物B的名称为 。
(2)物质A、C的关系为 。
a.同系物 b.同分异构体 c.同素异形体 d.分子式相差1个CH2
(3)①~④反应中,属于加成反应的有 。
(4)反应②的化学方程式为 。
(5)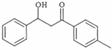 的同分异构体有许多。能与NaHCO3反应,且含有联苯基(
的同分异构体有许多。能与NaHCO3反应,且含有联苯基(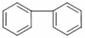 上1个氢原子被取代)的同分异构体共有 种。
上1个氢原子被取代)的同分异构体共有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:
把一定质量的铁完全溶解于某浓度的硝酸中收集到0.3 mol NO2和0.2 mol NO。向反应后的溶液中加入足量NaOH溶液充分反应,经过滤、洗涤后,把所得沉淀加热至质量不再减少为止。得到固体质量不可能为
A.18 g  B.24 g C.30 g D.36 g
B.24 g C.30 g D.36 g
查看答案和解析>>
科目:高中化学 来源: 题型:
正溴丁烷(CH3CH2CH2CH2Br)是一种重要的有机合成工业原料。在实验中可利用下图装置(加热或夹持装置省略)制备正溴丁烷。

制备时的化学反应方程式及有关数据如下:
NaBr+H2SO4=HBr+NaHSO4
C4H9OH+HB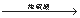 rC4H9Br+H2O
rC4H9Br+H2O
| 物质 | 相对分子质量 | 密度/g·cm-3 | 沸点/℃ | 水中溶解性 |
| 正丁醇 | 74 | 0.80 | 117.3 | 微溶 |
| 正溴丁烷 | 137 | 1.27 | 101.6 | 难溶 |
| 溴化氢 | 81 | --- | --- | 极易溶解 |
实验步骤:在装置A中加入2mL水,并小心加入28mL浓硫酸,混合均匀后冷却至室温。再依次加入18.5mL正丁醇和26g溴化钠,充分摇振后加入沸石,连接气体吸收装置C。将装置A置于石棉网上加热至沸腾,然后调节为小火使反应物保持平稳地回流。一段时间后停止加热,待反应液冷却后,拆去装置B,改为蒸馏装置,蒸出粗正溴丁烷。
请回答下列问题;
(1)仪器A的名称是________,仪器B的作用是________.操作中加入沸石的作用是________.
(2)装置C中盛装的液体是_______________,其作用是____________________.
(3)制备的粗产物正溴丁烷中往往含有水分、正丁醇等杂质,加入干燥剂出去水分后,再由下列操作中的___________制备纯净的正溴丁烷。
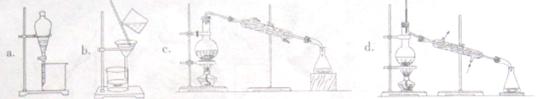
(4)若制备实验的“回流”过程中不采用“调节为小火”,仍采用大火加热回流,则会使产品产率偏_________(填“高”或“低”),试说出其中一种原因:_________________________.
(5)若最终得到13.6g纯净的正溴丁烷,则该实验的产率是_______________(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
己二酸是一种重要的有机二元酸,主要用于制造尼龙66纤维和尼龙66树脂,在实验室中可通过环己醇的氧化反应来制备。反应原理:
 +8HNO3
+8HNO3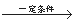 3HOOC(CH2)4COOH+8NO
3HOOC(CH2)4COOH+8NO +7H2O,反应装置(部分夹持装置和热源已省略)如图所示。
+7H2O,反应装置(部分夹持装置和热源已省略)如图所示。
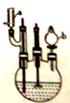
实验步骤:
I.在60mL三颈烧瓶中加入16.0mL50%硝酸(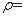 1.31g·cm-1)和微量(0.01g)偏钒酸铵,瓶的正口安装电动搅拌器,两侧口分别安装仪器a和b。用仪器b滴加5.3mL环己醇,搅拌器用玻璃搅拌棒,仪器a另一端连接气体吸收装置,用纯碱液作吸收溶液。
1.31g·cm-1)和微量(0.01g)偏钒酸铵,瓶的正口安装电动搅拌器,两侧口分别安装仪器a和b。用仪器b滴加5.3mL环己醇,搅拌器用玻璃搅拌棒,仪器a另一端连接气体吸收装置,用纯碱液作吸收溶液。
II.首先将瓶内液体加热到50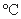 左右,开动搅拌器,滴入环己醇(
左右,开动搅拌器,滴入环己醇(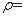 0.9624g·cm-1),使反应处于微沸状态,滴加完毕后于90
0.9624g·cm-1),使反应处于微沸状态,滴加完毕后于90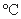 左右水浴加热20分钟,至反应完毕。
左右水浴加热20分钟,至反应完毕。
III.趁热倒出瓶中混合液于烧杯内,烧杯置于冰水浴中,静置冷却,析出产品,过滤,用少量冷水洗涤沉淀,干燥后称重。
IV.将粗产品在水中进行重结晶操作。
请回答下列问题:
(1)仪器a的名称是_________________。仪器b在使用前应_________________。
(2)偏钒酸铵的作用是_______________。
(3)反应完成后,趁热倒出反应液的目的是___________________。
(4)本实验中己二酸的理论产量为______________g。
(5)用纯碱液吸收尾气时发生的相关化学反应为:
2NO2+Na2CO3=NaNO2+NaNO3+CO2 ①
NO+NO2+Na2CO3=2NaNO2+NaNO3+CO2 ②
现用1000g质量分数为21.2%的纯碱吸收液吸收尾气,每产生22.4L(标准状况下)CO2 时,吸收液质量就增加44g,则吸收液中NaNO2和NaNO3的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.碳酸钙与盐酸反应:CO32-+2H+===H2O+CO2↑
B.硫酸氢钠溶液中加入足量的烧碱溶液:HSO4-+OH-=== SO42-+H2O
C.过氧化钠与水反应:2O22-+2H2O===4OH- + O2↑
D.澄清石灰 水中通入少量二氧化碳:Ca2++2OH-+CO2===CaCO3↓+H2O
水中通入少量二氧化碳:Ca2++2OH-+CO2===CaCO3↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com