
| 元素 | 有关信息 |
| A | 最高价氧化物对应的水化物与其氢化物反应生成离子化合物 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 原子最外层电子数比次外层电子数少1个 |
| E | 单质既可与盐酸反应,又可与NaOH溶液反应 |
| ||
| 7 |
| 14 |
| 16 |
| 16 |
| ||
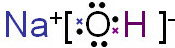 离子键 共价键 Cl2+2NaOH=NaCl+NaClO+H2O;
离子键 共价键 Cl2+2NaOH=NaCl+NaClO+H2O;

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案科目:高中化学 来源: 题型:
| A、常温常压下3.2 g O2中含有的氧原子数目为0.2 NA |
| B、101 kPa 0℃时,22.4 L氢气中含有NA个氢原子 |
| C、标准状况下,2.24 L 四氯化碳含有的碳原子数目为0.1NA |
| D、标准状况下,22.4LCl2和HCl的混合气体所含分子总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、检验C2H5Br中的Br元素时,将C2H5Br和NaOH溶液混合加热后,加硫酸酸化 |
| B、为提高KMnO4溶液的氧化能力,用浓盐酸将KMnO4溶液酸化 |
| C、检验蔗糖在稀硫酸中水解产生的葡萄糖,应先用NaOH溶液碱化后才能进一步检验 |
| D、检验溶液中是否含有SO42-时,先加氯化钡溶液后,再加稀盐酸酸化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
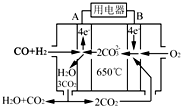
 金属(M)的腐蚀是因为发生反应:M-ne-→Mn+.金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁的腐蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.
金属(M)的腐蚀是因为发生反应:M-ne-→Mn+.金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁的腐蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| 1000°C |
| ═ |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
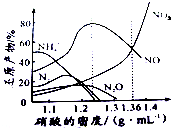
 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
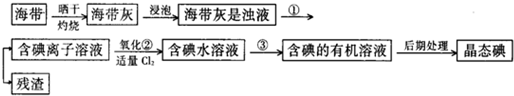
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com