
分析 电解质是水溶液中或熔融状态下都导电的化合物;非电解质是水溶液中和熔融状态下都不导电的化合物,据此解答.
解答 解:①液氨是液态氨气,本身不能电离,溶于水能导电的原因是与水化合生成一水合氨,液氨是非电解质;
②MgCl2晶体属于盐,溶于水或熔融状态下均能导电,属于电解质;
③液态的醋酸是酸,不能导电,溶于水能导电,属于电解质;
④汞能导电,是金属单质,既不是电解质也不是非电解质;
⑤BaCO3固体不能导电,熔融状态下能导电,属于电解质;
⑥矿泉水能导电,属于混合物,既不是电解质也不是非电解质;
⑦酒精(C2H5OH)不能导电,属于非电解质;
⑧熔化的KOH能导电,是碱,属于电解质;
⑨硫酸溶液能导电,是混合物,既不是电解质也不是非电解质;
⑩干冰本身不能电离,属于非电解质,
故答案为:(1)④⑥⑧⑨;
(2)②③⑤⑧;
(3)①⑦⑩;
(4)⑥⑨.
点评 本题考查了电解质、非电解质的判断,熟悉相关概念是解题关键,注意电解质必须是本身能够电离,电解质导电需要条件,题目难度不大.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2CO3加在BaCl2前 | B. | Na2CO3加在BaCl2后 | ||
| C. | 同时加 | D. | 无固定顺序 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
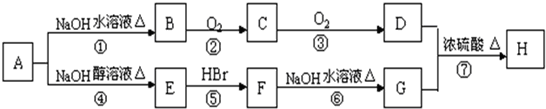
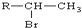 (R为烃基)
(R为烃基) .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属腐蚀就是金属原子失去电子被还原的过程 | |
| B. | 钢铁吸氧腐蚀时,负极反应式为2H2O+O2+4e-═4OH- | |
| C. | 向醋酸钠溶液中加入适量醋酸至混合液pH=7时,溶液中c(Na+)=c(CH3COO-) | |
| D. | 0.1 mol/L NH4Cl溶液中,c(NH${\;}_{4}^{+}$)+c(H+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
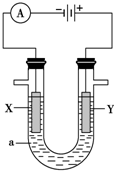 电解原理在化学工业中有广泛的应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g金属钠 | B. | 1mol/L BaCl2溶液100mL | ||
| C. | 56g金属铁 | D. | 20% NaOH溶液50g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
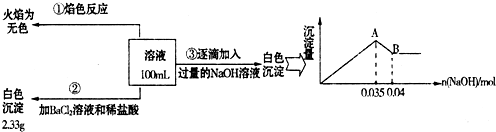
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
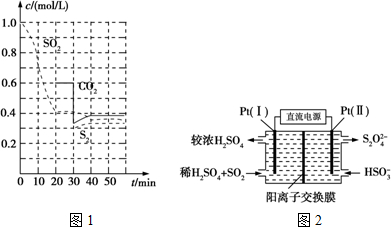
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com