
下列各项中的两个量,其比值一定为2:1的是
A.液面在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体
B.在碳与浓硫酸的反应中,还原产物与氧化产物的物质的量
C.1mol Na2O2与1molNa2O中的阴离子数目
D.相同温度下,0.2mol/L醋酸溶液和0.1mol/L醋酸溶液中c(H+)
B
【解析】
试题分析:A、滴定管的下端有部分无刻度,所以液面在“0”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体体积比不是2:1,错误;B、C与浓硫酸的反应为C+2H2SO4(浓)  CO2↑+2SO2↑+2H2O,氧化产物是二氧化碳,还原产物是二氧化硫,所以还原产物与氧化产物的物质的量比是2:1,正确;C、1mol Na2O2与1molNa2O中的阴离子数目相同,都是1mol,错误;D、醋酸是弱酸,溶液越稀电离度越大,所以0.2mol/L的醋酸溶液和0.1mol/L醋酸溶液中c(H+)之比小于2:1,错误,答案选B。
CO2↑+2SO2↑+2H2O,氧化产物是二氧化碳,还原产物是二氧化硫,所以还原产物与氧化产物的物质的量比是2:1,正确;C、1mol Na2O2与1molNa2O中的阴离子数目相同,都是1mol,错误;D、醋酸是弱酸,溶液越稀电离度越大,所以0.2mol/L的醋酸溶液和0.1mol/L醋酸溶液中c(H+)之比小于2:1,错误,答案选B。
考点:考查物质的粒子数比是判断,滴定管内液体体积的判断


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:2014-2015陕西省宝鸡市高一上学期期末化学试卷(解析版) 题型:选择题
关于基本营养物质的说法正确的是
A.所有蛋白质均可通过颜色反应来鉴别
B.葡萄糖和蔗糖不是同分异构体,但属于同系物
C.糖类、油脂、蛋白质都是由C、H、O三种元素组成的
D.油脂在酸性条件下水解为丙三醇和高级脂肪酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列化学事实的描述或解释正确的是
A.Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)===c(OH-)
B.NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-==CO32-+H2O
C.有些化学反应既属于复分解反应又属于氧化还原反应
D.常温下,将pH=3的HA和PH=11的BOH等体积混合后PH>7,可能生成了弱酸强碱盐
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
将浓度为0.1 mol·L-1 HF溶液加水不断稀释,下列各量始终保持增大的是
A.c(H+) B.Ka(HF) C.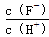 D.
D.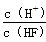
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴彦淖尔市高三上学期期中考试化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(气) + Y2(气)  2Z(气), 已知 X2、Y2、Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当反应达到平衡时, 各物质的浓度不可能的是
2Z(气), 已知 X2、Y2、Z的起始浓度分别为 0.1 mol/L, 0.3 mol/L, 0.2 mol/L, 在一定的条件下, 当反应达到平衡时, 各物质的浓度不可能的是
A.Z 为 0.3 mol/L B.Y2 为 0.35 mol/L
C.X2 为 0.12 mol/L D.Z 为 0.4 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
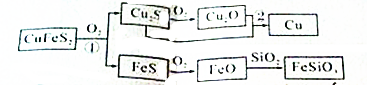
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,pH=4.7浓度均为0.1mol?L-1的CH2COOH、CH3COONa混合溶液中,c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+) |
| B、常温下,氨水与(NH4)2SO4溶液混合所得pH=7的溶液中,c(NH4+):c(SO42-)=2:1 |
| C、将体积相同,pH均为1的盐酸和醋酸分别加水稀释至pH=3,盐酸的体积变化大,证明醋酸是弱酸 |
| D、向2.0ml浓度均为0.1mol?L-1的KCl、KI混合液中滴加1-2滴0.01mol?L-1AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
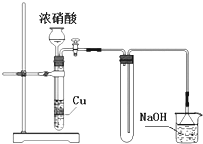
| A、用广泛pH试纸测得0.051 mol?L-1 H2SO4溶液的pH=1 |
| B、某气体制备装置如右图,该装置可减少污染性气体的泄漏,且有利于收集到空气含量较低的气体 |
| C、在分液操作中,当试液分层后,打开旋塞,将下层液体放出,然后关闭旋塞,将上层液体从上口倒出 |
| D、10mL溴水与5mL正己烷混合,在光照下振荡后静置,当试液分为上、下两层且几乎无色时,用玻璃棒蘸取浓氨水伸入液面上方,可观察到有白烟生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com