
| A. | (b-2a)/3mol•L-1 | B. | (b-2a)/2mol•L-1 | C. | (2b-a)/3mol•L-1 | D. | (2b-a)/2 mol•L-1 |
分析 溶液中满足电荷守恒,根据电荷守恒可知:3c(Al3+)+c(NH4+)=2c(SO42-),据此进行计算原混合溶液中钾离子的物质的量浓度.
解答 解:溶液中NH4+的物质的量浓度为amol•L-1,SO42-的物质的量浓度为bmol•L-1,
根据溶液电荷守可知:3c(Al3+)+c(NH4+)=2c(SO42-),
即:3c(Al3+)+amol•L-1=2×bmol•L-1,
解得:c(Al3+)=$\frac{2b-a}{3}$mol•L-1,
故选C.
点评 本题考查混合溶液中离子物质的量浓度的计算,题目难度中等,注意溶液中离子浓度计算中电荷守恒的运用,试题侧重考查学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
 在金属或非金属底物材料上,用NaBH4进行“化学镀”镀镍,可以得到坚硬、耐腐蚀的保护层(3Ni3B+Ni),反应的离子方程式为:20Ni2++16BH4-+34OH-+6H2O═2(3Ni3B+Ni)+10B(OH)4-+35H2↑
在金属或非金属底物材料上,用NaBH4进行“化学镀”镀镍,可以得到坚硬、耐腐蚀的保护层(3Ni3B+Ni),反应的离子方程式为:20Ni2++16BH4-+34OH-+6H2O═2(3Ni3B+Ni)+10B(OH)4-+35H2↑查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z 为 0.4mol•L-1 | B. | X 为 0.2 mol•L-1 | ||
| C. | Y 为 0.4 mol•L-1 | D. | Z 为 0.3 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中含有1mol的Na2SO4 | |
| B. | 从1L溶液中取出500 mL后,剩余溶液的浓度变为0.5mol/L | |
| C. | 1mol的Na2SO4 溶于1L水 | |
| D. | 1L溶液中含有142 g Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 30% | B. | 10% | C. | 20% | D. | 24% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
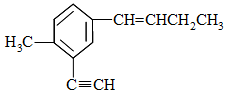
| A. | 与乙苯不互为同系物 | |
| B. | 分子中共直线的碳原子最多有4个 | |
| C. | 分子中共平面的原子最多有20个 | |
| D. | 与其互为同分异构体且萘环上只有一个侧链的共有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散质的粒子是否为大量分子或离子的集合体 | |
| B. | 能否透过滤纸 | |
| C. | 分散质粒子直径的大小 | |
| D. | 是否均一、稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5 NA | |
| B. | 标准状况下,11.2 L H2O 中含有的分子数目为0.5NA | |
| C. | 0.10 mol Fe 粉与足量水蒸气反应生成的H2分子数为0.10 NA | |
| D. | 25℃,1.01×105Pa,64gSO2中含有的原子数为3 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com