
【题目】以硅石(主要成分SiO2)为起始原料生产高纯多晶硅的简化工艺流程如下图所示:
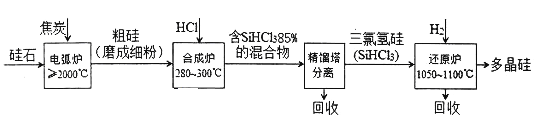
(1)在电弧炉中,生成粗硅的化学方程式为____________,该反应氧化剂与还原剂物质的量之比为_____________。
(2)合成炉中有关反应的数据如下表所示:
热化学方程式 | 平衡常数 | |
主反应 | Si(s)+3HCl(g) | K1 |
副反应 | Si(s)+4HCl(g) | K2 |
①主反应的温度需严格控制在280~300℃之间,若温度过低,则__________________;若温度太高,SiHCl3则会转化生成SiCl4,该转化的热化学方程式为_____________________。
②平衡时,![]() 的值a随着
的值a随着![]() 的值b的变化而变化,则
的值b的变化而变化,则![]() =______(用含K1、K2的代数式表示)。工业上用H2适当稀释HCl来提高
=______(用含K1、K2的代数式表示)。工业上用H2适当稀释HCl来提高![]() 的值,请用平衡移动原理加以解释________________________。
的值,请用平衡移动原理加以解释________________________。
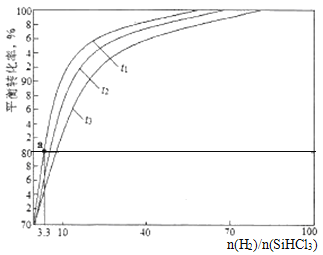
(3)还原炉中的主要反应为SiHCl3(g)+H2(g)=Si(s)+3HCl(g) △H>0。实验室中在1.0L密闭容器中研究得到SiHCl3的转化率在不同温度条件下随n(H2)/(SiHCl3)变化的曲线如图所示。t1、t2、t3表示的温度高低顺序为_______;t1温度时平衡常数Ka=______(保留两位小数)。
【答案】SiO2+2C![]() Si+2CO↑ 1:2 反应速率慢,达到平衡需要时间长,物质的平衡含量低,生产效率低下 SiHCl3(g)+ HCl(g)
Si+2CO↑ 1:2 反应速率慢,达到平衡需要时间长,物质的平衡含量低,生产效率低下 SiHCl3(g)+ HCl(g)![]() SiCl4(g)+H2(g) △H=-31kJ/mol
SiCl4(g)+H2(g) △H=-31kJ/mol ![]() 增大c(H2)浓度,平衡逆向移动,可降低c(SiCl4)的浓度,增大c(SiHCl3)的浓度从而使
增大c(H2)浓度,平衡逆向移动,可降低c(SiCl4)的浓度,增大c(SiHCl3)的浓度从而使![]() 增大 t1>t2>t3 76.80
增大 t1>t2>t3 76.80
【解析】
(1)根据二氧化硅和焦炭在高温的条件下生成硅和一氧化碳进行分析;并根据氧化还原反应的规律判断氧化剂、还原剂;
(2)①从反应速率和物质平衡含量与温度的关系分析;
②利用平衡常数定义与a、b关系分析判断;
(3)根据该反应的正反应为吸热反应,从温度对物质平衡转化率影响分析;运用三段式法计算a点的化学平衡常数。
(1)二氧化硅和焦炭在高温的条件下生成硅和一氧化碳,化学方程式为:SiO2+2C![]() Si+2CO↑;在该反应中C元素化合价升高,失去电子,作还原剂,SiO2中的Si元素化合价降低,获得电子,SiO2作氧化剂,所以氧化剂与还原剂的物质的量的比为1:2;
Si+2CO↑;在该反应中C元素化合价升高,失去电子,作还原剂,SiO2中的Si元素化合价降低,获得电子,SiO2作氧化剂,所以氧化剂与还原剂的物质的量的比为1:2;
(2) ①温度过低,反应速率慢,达到平衡所需要的时间太久,不经济;且主反应的正反应为吸热反应,降低温度,平衡逆向移动,产生的SiHCl3的物质的量偏少,所以要在一定温度下进行;但若温度过高,又会发生副反应,SiHCl3又会转化生成SiCl4,使需要的物质产率降低;将副反应与主反应两式相减,整理可得SiHCl3(g)+ HCl(g)![]() SiCl4(g)+H2(g) △H=-31kJ/mol
SiCl4(g)+H2(g) △H=-31kJ/mol
②根据热化学方程式可得K1=![]() ,K2=
,K2=![]() ,
,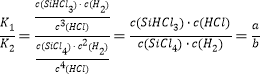 ,即
,即![]() ;由于K1、K2都是常数,所以从
;由于K1、K2都是常数,所以从![]() 等于常数可知:适当增大c(H2),化学平衡 SiHCl3(g)+ HCl(g)
等于常数可知:适当增大c(H2),化学平衡 SiHCl3(g)+ HCl(g)![]() SiCl4(g)+H2(g)逆向移动,使容器中c(SiCl4)减小,c(SiHCl3)增大,这样
SiCl4(g)+H2(g)逆向移动,使容器中c(SiCl4)减小,c(SiHCl3)增大,这样![]() 就会增大,从而降低了副产物的产生,得到更多SiHCl3,提高了产品的产率和生产效率;
就会增大,从而降低了副产物的产生,得到更多SiHCl3,提高了产品的产率和生产效率;
(3)根据图象可知:当其它条件相同而温度不同的情况下,物质SiHCl3的转化率:t1>t2>t3。由于该反应的正反应为吸热反应,在其他条件不变的条件下,升高温度,化学平衡正向移动,SiHCl3转化率提高,所以温度大小关系为:t1>t2>t3;
在a点时假设n(SiHCl3)=1mol,则n(H2)=3.3mol,由于容器的容积是1.0L,故开始时c(SiHCl3)=1mol/L, c(H2)=3.3mol/mol,用三段式进行计算:
SiHCl3(g)+H2(g)=Si(s)+3HCl(g)
c(开始)mol/L 1 3.3 0
c(变化) mol/L 0.8 2.4 2.4
c(平衡) mol/L 0.2 0.9 2.4
则K=![]()


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①H2(g)+1/2O2(g)![]() H2O(l) ΔH=285.8 kJ·mol1
H2O(l) ΔH=285.8 kJ·mol1
②H2(g)+1/2O2(g)![]() H2O(g) ΔH=241.8 kJ·mol1
H2O(g) ΔH=241.8 kJ·mol1
③C(s)+ 1/2O2(g)![]() CO(g) ΔH=110.5 kJ·mol1
CO(g) ΔH=110.5 kJ·mol1
④C(s)+O2(g)![]() CO2(g) ΔH=393.5 kJ·mol1
CO2(g) ΔH=393.5 kJ·mol1
回答下列各问题:
(1)上述反应中属于放热反应的是_______________________。
(2)H2的燃烧热为________
(3)燃烧10 g H2生成液态水,放出的热量为________。
(4)CO的燃烧热为________;其热化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“钙基固硫”是将煤中的硫元素以CaSO4的形式固定脱硫,而煤炭燃烧过程中产生的CO又会发生反应I和反应II,导致脱硫效率降低。某温度下,反应I的速率(v1)大于反应II的速率(v2),则下列反应过程能量变化示意图正确的是
反应I:CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ·mol-1
CaO(s)+SO2(g)+CO2(g) △H1=+218.4kJ·mol-1
反应II:CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) △H2=-175.6kJ·mol-1
CaS(s)+4CO2(g) △H2=-175.6kJ·mol-1

A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸铁锂电池是新型的绿色能源电池,其简化的生产工艺流程如下。
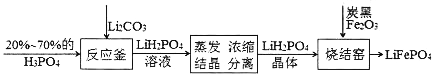
(1)反应釜中反应的化学方程式为_______,该反应体现出非金属性关系:P_____C(填“>”或“<”)。
(2)室温下,LiH2PO4溶液的pH随c(H2PO4-)的变化如图1所示,H3PO4溶液中H2PO4-的分布分数![]() 随pH的变化如图2所示[
随pH的变化如图2所示[![]() (含P元素的粒子)]。
(含P元素的粒子)]。
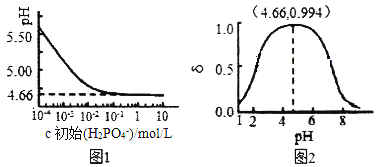
①由图1知,低浓度时LiH2PO4溶液的pH小于7,且随着c初始(H2PO4-)的增大而减小,其合理的解释为__________________。
②综合上图分析,若用浓度大于1mol/L的H3PO4溶液溶解Li2CO3,要使反应釜中的H3PO4几乎全部转化成LiH2PO4,反应釜中需要控制溶液的pH=________。
(3)磷酸铁锂电池总反应为:LiFePO4+6C![]() Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向______(填“阳极”或“阴极”);放电时,正极反应式为__________________。
Li1-xFePO4+LixC6,电池中的固体电解质可传导Li+。充电时,Li+移向______(填“阳极”或“阴极”);放电时,正极反应式为__________________。
(4)磷酸铁锂电池中铁的含量可通过如下方法测定:称取1.60g试样用盐酸溶解,在溶液中加入稍过量的SnCl2溶液,再加入HgCl2饱和溶液,用二苯胺磺酸钠作指示剂,用0.030mol/L重铬酸钾溶液滴定至溶液由浅绿色变为蓝紫色,消耗重铬酸钾溶液50.00mL。
已知:2Fe3++Sn2++6Cl-=SnCl62-+2Fe2+
4Cl-+Sn2++2HgCl2=SnCl62-+Hg2Cl2
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
①实验中加入HgCl2饱和溶液的目的是____________。
②铁的百分含量Fe(%)=_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝土矿是冶炼金属铝的重要原料,其中主要成分为 Al2O3、Fe2O3 等。工业上可 NaOH 溶解 Al2O3 使 其与杂质分离:Al2O3+2NaOH═2NaAlO2+H2O
(1)找出上述反应中化合价为负值的元素,写出其原子的电子式_____。
(2)同温同压下,上述元素形成的气体密度最大的物质的分子式为_____。
(3)上述反应中两种金属元素对应单质的活泼性强弱关系为:____,从原子结构的角度分 析其原因:_________。
(4)若根据化学性质进行物质分类,则 Al2O3 属于______氧化物,据此推测下列反应方程式正确的是______。
A.Al2O3+3H2O═2Al(OH)3
B.2Al(OH)3+3H2SO4═Al2(SO4)3+3H2O
C.Al(OH)3+NaOH═NaA1O2+2H2O
D NaAlO2+4HCl═AlCl3+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1L0.2mol/LKMnO4酸性溶液与一定量pH=3的草酸(HOOC-COOH)溶液混合,放出VL气体。NA代表阿伏加德罗常数的值,下列说法正确的是
A. pH=3的草酸溶液含有H+数目为0.001NA
B. 当1molKMnO4被还原时强酸提供H+数目为NA
C. 1molHOOC-COOH含共用电子对数目为9NA
D. 该反应释放CO2分子数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜、磷及其化合物是非常重要的物质。
(1)Cu+的电子排布式____;
(2)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-。[Cu(CN)4]2-的配体为____,[Cu(CN)4]2-中C的杂化方式为____,则1个[Cu(CN)4]2-中含有的σ键的数目为____个;
(3)锂—磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,不溶于水,可通过Na3PO4、CuSO4和NH3·H2O反应制取。制取Cu4O(PO4)2的化学方程式为____;
(4)PCl5中P-Cl键长有198pm和206pm两种。PCl5是非极性分子,可作为导电熔体,其原理为PCl5电离为一个阴离子和一个阳离子,其中阴离子为正八面体,阳离子为正四面体,写出一种阳离子的等电子体的化学式____,PCl5的立体构型为____;
(5)金属铜属于面心立方晶体,铜的密度为ag·cm3,NA表示阿伏伽德罗常数,则铜的配位数____,铜的金属半径为___pm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com