
分析 (1)①假设I:NO2氧化Na2O2;则Na2O2中氧元素化合价升高生成氧气,NO2中氮元素化合价降低生成盐,有反应生成一种盐和一种气体单质,假设Ⅱ:反应只生成一种盐,说明氮元素化合价升高,Na2O2中氧元素化合价降低,则该假设为过氧化钠氧化NO2;
②过氧化钠与水蒸气反应生成氧气;
③假设II正确,根据化合价升降变化和质量守恒书写可得;
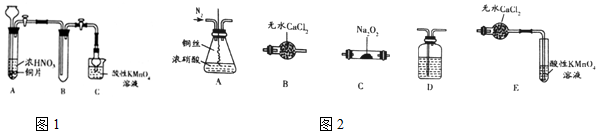
(2)①装置A中是浓硝酸和铜发生的反应,反应生成二氧化氮和水,装置D中将A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,通过装置B干燥生成的一氧化氮,在装置C中与过氧化钠反应,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气;
②二氧化氮与水反应可转化为一氧化氮;
③反应前通入氮气排除装置中的空气,反应后通氮气为排尽装置内的氮氧化物;
④装置E中试管内为NO与高锰酸根离子反应生成锰离子和硝酸根离子;
⑤根据题意,亚硝酸钠与稀硫酸反应生成NO气体,NO遇氧气生成红棕色气体二氧化氮,据此分析.
解答 解:(1)①假设Ⅱ:反应只生成一种盐,说明氮元素化合价升高,Na2O2中氧元素化合价降低,则该假设为过氧化钠氧化NO2;
故答案为:过氧化钠氧化NO2;
②A装置制备的NO2气体中混有水蒸气,它能与过氧化钠反应产生氧气,使带火里的木条复燃,所以该装置不能证明氧气是否为二氧化氮与过氧化钠反应所得;
故答案为:NO2气体中混有水蒸气,它能与过氧化钠反应产生氧气,使带火里的木条复燃;
③假设II正确,说明氮元素化合价升高,Na2O2中氧元素化合价降低,则该假设为过氧化钠氧化NO2,生成硝酸钠,反应为:2NO2+Na2O2?2NaNO3;
故答案为:2NO2+Na2O2?2NaNO3;
(2)①装置A中是浓硝酸和铜发生的反应,反应生成二氧化氮和水,装置D中将A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,通过装置B干燥生成的一氧化氮,在装置C中与过氧化钠反应,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气,故连接顺序为:A、D、B、C、E;
故答案为:A、D、B、C、E;
②装置D的作用是将二氧化氮转化为一氧化氮,二氧化氮与水反应可得一氧化氮;
故答案为:c;
③NO易被氧化,故反应前通入氮气排除装置中的空气,反应后通氮气为排尽装置内的氮氧化物,防止污染空气;
故答案为:排尽装置中的空气;排尽装置中的氮氧化物;
④装置E中试管内为NO与高锰酸根离子反应生成锰离子和硝酸根离子,离子反应为:NO+3MnO4-+4H+=3Mn2++5NO3-+2H2O;
故答案为:NO+3MnO4-+4H+=3Mn2++5NO3-+2H2O;
⑤根据题意信息:6NaNO2+3H2SO4═3Na2SO4+2HNO3+4NO↑+2H2O,NO遇空气生成红棕色的二氧化氮,故方法为:取少量C中的固体于试管中,加入稀硫酸,产生无色气体,遇到空气变为红棕色,证明产物是亚硝酸钠;
故答案为:取C装置中产物少许于试管中,加入稀硫酸,开始产生无色气体,遇到空气变为红棕色,证明产物是亚硝酸钠.
点评 本题考查了物质制备实验方案的设计和信息判断,物质性质的理解应用,注意实验过程中的反应现象分析,掌握基础是关键,题目难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 12753I和13153I是质子数相同的同种核素 | |
| B. | 结构和组成相似的物质,沸点随相对分子质量增大而升高,所以NH3沸点低于PH3 | |
| C. | 实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 | |
| D. | 为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LCCl4中含有的分子数为0.5NA | |
| B. | 在Na2O2与水的反应中,每生成1molO2,转移电子数目为2NA | |
| C. | 常温常压下,等物质的量浓度的Na2CO3与Na2S溶液Na+数目相等 | |
| D. | 常温常压下,4.6g乙醇中含有极性共价键的数目为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 CO2经催化加氢可合成乙烯:2CO2 (g)+6H2(g)?C2H4(g)+4H2O(g).0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图.下列叙述不正确的是( )
CO2经催化加氢可合成乙烯:2CO2 (g)+6H2(g)?C2H4(g)+4H2O(g).0.1MPa时,按n(CO2):n(H2)=l:3投料,测得不同温度下平衡时体系中各物质浓度的关系如图.下列叙述不正确的是( )| A. | 该反应的△H<O | |
| B. | 曲线b代表H2O | |
| C. | N点和M点所处状态的c(H2)不一样 | |
| D. | 其它条件不变,T1℃、0.2 MPa下反应达平衡时c(H2)比M点大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下都不能用铝制容器贮存 | |
| B. | 滴在紫色石蕊试纸上,试纸都变黑 | |
| C. | 常温下都能与铜较快反应 | |
| D. | 露置在空气中,容器内酸液的浓度都降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地沟油经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | PM2.5颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶 | |
| C. | 采用纳米TiO2光触媒技术,可将装修材料中释放的HCHO转化为无害物质 | |
| D. | 神舟十一号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是硅晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol ICl溶于NaOH溶液中生成NaC1和NaIO时,转移的电子数为NA | |
| B. | 常温下,1 L PH=2的HC1溶液和1 L PH=1的CH3COOH溶液混合后,混合溶液中所含的氢离子数目大于0.11NA | |
| C. | 常温下,含有NA个NO2和N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L | |
| D. | 常里常压下,18g D2O中所含中子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28gN2所含原子数为NA | B. | 0.5molH2O所含原子数为1.5NA | ||
| C. | 1molH2O含有的水分子数目为NA | D. | 0.5NACl2分子的物质的量是0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯佐卡因( )是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2 )是局部麻醉药,分子中含有2种官能团,分子式为C9H10NO2 | |
| B. | 香叶醇( )能发生加成反应不能发生取代反应 )能发生加成反应不能发生取代反应 | |
| C. | 青蒿素( ) 的一氯代物有5种(不含立体异构) ) 的一氯代物有5种(不含立体异构) | |
| D. | 某有机物的分子式为C4H8,能使溴的CCl4溶液褪色,则它在一定条件下与水反应时最多可生成的有机物(不考虑立体异构)有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com