
| A. | HF的热稳定性很好,是因为HF分子间存在氢键 | |
| B. | 构成单质分子的粒子之间不一定存在共价键 | |
| C. | 由非金属元素组成的化合物不一定是共价化合物 | |
| D. | 阴、阳离子间通过离子键一定能形成离子化合物 |
分析 A、稳定性是化学性质,而氢键是决定物理性质;
B、如稀气体之间不存任何化学键;
C、氯化铵是由非金属元素组成,而氯化铵是共价化合物;
D、离子键是阴阳离子之间形成的化学键.
解答 解:A、稳定性是化学性质,而氢键是决定物理性质,而氟化氢稳定是氢氟键的键能大,故A错误;
B、如稀气体之间不存任何化学键,所以构成单质分子的粒子之间不一定存在共价键,故B正确;
C、氯化铵是由非金属元素组成,而氯化铵是共价化合物,所以由非金属元素组成的化合物不一定是共价化合物,故C正确;
D、离子键是阴阳离子之间形成的化学键,故D正确;
故选A.
点评 本题考查氢键及氢键对物质的性质的影响,明确氢键、范德华力、化学键的不同及对物质的性质的影响即可解答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 邻二甲苯只有一种结构,能证明苯环中不存在碳碳单键和碳碳双键交替的结构 | |
| B. | 高聚物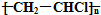 的单体可以通过乙烯和HCl加成制得 的单体可以通过乙烯和HCl加成制得 | |
| C. | (CH3)2CH-CH=CH-C(CH3)3与氢气加成后的产物用系统命名法命名为2,2,5-三甲基己烷 | |
| D. | 完全燃烧一定质量的冰醋酸、葡萄糖混合物(以任意质量比混合),生成CO2和H2O的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①②④ | C. | ④⑤ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
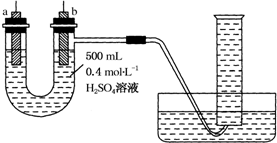 实验室提供纯锌、纯铜片和500mL 0.4mol•L-1的H2SO4溶液、导线、1 000mL量筒.试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量.
实验室提供纯锌、纯铜片和500mL 0.4mol•L-1的H2SO4溶液、导线、1 000mL量筒.试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>D>C | B. | A>C>D>B | C. | C>A>B>D | D. | B>D>C>A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 被提纯物质 | 除杂试剂 | 分离方法 |
| ① | 苯甲酸(不溶于水的杂质) | 水 | 过滤、重结晶 |
| ② | 乙酸乙酯(醋酸) | 氢氧化钠溶液 | 分液 |
| ③ | 乙醇(4%的水) | 生石灰 | 蒸馏 |
| ④ | 二氧化碳(氯化氢) | 饱和碳酸钠溶液 | 洗气 |
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、SO42-、CO32- | B. | NH4+、Mg2+、SO32-、Cl- | ||
| C. | Na+、K+、HCO3-、Cl- | D. | K+、Cu2+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
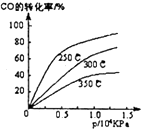 工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题:
工业合成甲醇反应如下:CO(g)+2H2(g)?CH3OH(g);△H请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
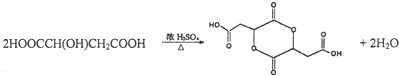 .
.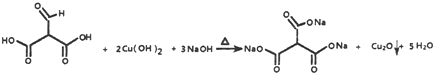 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com