
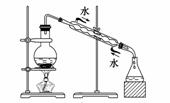
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是
 |
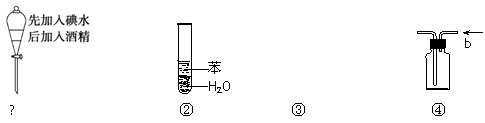 |
A.溶液上层无色,下层紫红色
B.装置②可用于吸收HCl气体,并防止倒吸
 C.装置③可用于制取蒸馏水
C.装置③可用于制取蒸馏水
D.装置④ b口进气可收集H2、CO2等气体
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列相关反应的离子方程式书写正确的是( )
A.4molFe 在5molCl2中点燃反应:5Cl2+4Fe=2FeCl2+2FeCl3
B.氯化铁溶液中通入硫化氢:2Fe3++H2S=2Fe2++S↓+2H+
C.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:
2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学用语的表示正确的是
A.过氧化钠的电子式: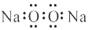 B.质子数为35、中子数为45的溴原子:
B.质子数为35、中子数为45的溴原子: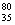 Br
Br
C.硫离子的结构示意图: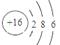 D.乙烯的结构简式:CH2CH2
D.乙烯的结构简式:CH2CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C处分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等,下列说法正确的是
A.X的相对分子质量等于Y的相对分子质量
B.X的相对分子质量比Y的相对分子质量小
C.气体的体积:V(X)>V(H2)>V(Y)
D.物质的量:n(X)<n(H2)<n(Y)
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ. 过氧化氢(H2O2)的水溶液俗称双氧水,近年来倍受人们的青睐,被称为“绿色氧化剂”。
(1)写出H2O2的电子式_________________
(2)你认为H2O2被称为“绿色氧化剂”的主要原因是______________________________
(3)将双氧水加入用盐酸酸化的FeCl2溶液中,溶液由浅绿色变为棕黄色,写出该反应的离子方程式为_________________________________,反应中H2O2作_____________剂
(4)双氧水能使酸性高锰酸钾溶液褪色,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里:
MnO4-+___H2O2+_____H+ ===_____Mn2++____H2O+ 。
Ⅱ. 某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2,已知该反应中H2O2只发生如下过程:H2O2→ O2
⑴该反应的化学方程式为________________________________________________________
⑵如反应转移了0. 3mol电子,则产生的气体在标准状况下体积为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
B.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
C.根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
D.使用静电除尘器除去空气中的飘尘利用了胶体的性质
查看答案和解析>>
科目:高中化学 来源: 题型:
工业制ClO2的化学反应:2NaClO3 + SO2 + H2SO4=2ClO2 + 2NaHSO4,下列说法正确的是
A.NaClO3在反应中化合价降低,失去电子
B.SO2在反应中发生氧化反应
C.1 mol氧化剂在反应中得到2 mol电子
D.H2SO4 在反应中作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,混合后 得到密度为1.17 g·cm-3的溶液。请计算:
得到密度为1.17 g·cm-3的溶液。请计算:
(1)混合后溶液中NaCl的质量分数为________。
(2)混合后溶液中NaCl的物质的量浓度为________。
(3)在1 000 g水中需加入________mol NaCl,才能使其浓度恰好与上述混合后溶液的浓度相等。(假设密度不变,计算结果保留1位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸盐在能源、环保等方面有着广泛的用途。高铁酸钾(K2FeO4)易溶于水,具有强氧化性,是一种新型水处理剂。替代传统的净水剂及Cl2对淡水进行净化消毒是城市饮用水处理新技术。
工业上常用如下方法制备高铁酸钾:以铁丝网为阳极电解NaOH溶液,然后在阳极液中加入50%的KOH溶液,充分反应后,过滤、用异丙醇洗涤、干燥,即可制得。
(1)高铁酸钾具有强氧化性的原因是 ▲ 。
(2)用异丙醇代替水洗涤产品的好处是 ▲ 。
(3)高铁酸钾是一种理想的水处理剂,其处理水的原理为 ▲ , ▲ 。
(4)高铁电池是正在研制中的可充电干电池,下图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 ▲ 、 ▲ 。
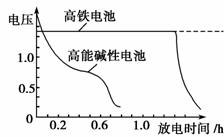
(5)探究高铁酸钾的某种性质。
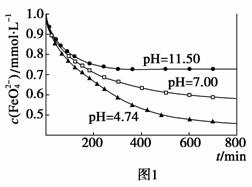 [实验1]将适量K2FeO4固体分别溶解于pH为4.74、7.00、11.50的水溶液中,配得FeO
[实验1]将适量K2FeO4固体分别溶解于pH为4.74、7.00、11.50的水溶液中,配得FeO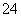 浓度为1.0 mmol·L-1(1 mmol·L-1=10-3 mol·L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
浓度为1.0 mmol·L-1(1 mmol·L-1=10-3 mol·L-1)的试样,静置,考察不同初始pH的水溶液对K2FeO4某种性质的影响,结果见图1(注:800 min后,三种溶液中高铁酸钾的浓度不再改变)。
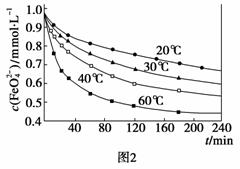
[实验2]将适量K2FeO4溶解于pH=4.74的水溶液中,配制成FeO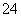 浓度为1.0 mmol·L-1的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
浓度为1.0 mmol·L-1的试样,将试样分别置于20 ℃、30 ℃、40 ℃和60 ℃的恒温水浴中,考察不同温度对K2FeO4某种性质的影响,结果见图2。则
①实验1的目的是 ▲ ;
②实验2可得出的结论是 ▲ ;
③高铁酸钾在水中的反应为4FeO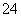 +10H2O
+10H2O 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。
由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com