
| A. | 澄清透明的无色溶液:MnO4-、Na+、I-、Mg2+ | |
| B. | 含有0.1mol/L Fe3+的溶液中:Na+、Ca2+、SCN-、SO42- | |
| C. | 与铝片反应产生氢气的溶液:CO32-、SO42-、Na+、NH4+ | |
| D. | 使酚酞溶液变红的溶液:Na+、Cl-、NO3-、Ba2+ |
分析 A.高锰酸根离子为有色离子,且高锰酸根离子能够氧化碘离子;
B.铁离子能够与硫氰根离子结合生成络合物硫氰化铁,钙离子与硫酸根离子生成微溶物硫酸钙;
C.该溶液中存在大量氢离子或氢氧根离子,碳酸根离子与氢离子反应,铵根离子与氢氧根离子反应;
D.该溶液呈碱性,四种离子之间不反应,都不与氢氧根离子反应.
解答 解:A.MnO4-为有色离子,且MnO4-、I-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.Fe3+、SCN-之间反应生成硫氰化铁,Ca2+、SO42-之间反应生成硫酸钙,在溶液中不能大量共存,故B错误;
C.与铝片反应产生氢气的溶液呈酸性或强碱性,CO32-与酸性溶液中的氢离子反应,NH4+与氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.该溶液中存在大量氢氧根离子,Na+、Cl-、NO3-、Ba2+之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存的判断,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用SO2漂白过的草帽日久会变色 | |
| B. | 用天燃气代替煤作燃料可减少大气污 | |
| C. | “84消毒液”杀死病菌是因为蛋白质变性 | |
| D. | 乙醇用作医用消毒剂时,无水乙醇消毒效果最好 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
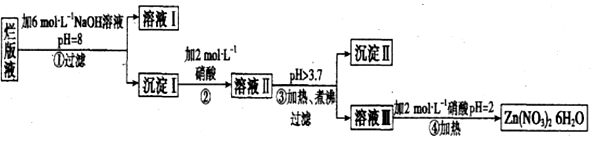
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②⑥⑦ | B. | 只有⑦ | C. | ④⑤⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与等体积pH=11的NaOH溶液混合后所得溶液显酸性 | |
| B. | c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L | |
| D. | 加入少量CH3COONa固体后,c(CH3COO-)降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A. | 含0.5 mol HCl的稀溶液与含 0.55 mol NaOH的稀溶液混合 | 测得放出热量为a kJ | 强酸与强碱反应的中和热为2a kJ/mol |
| B. | 向CuCl2、MgCl2的混合溶液中滴加NaOH溶液 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| C. | 将铁钉和铜丝用导线连接后放入滴有酚酞的氯化铵溶液中 | 铜丝附近溶液变红色 | 铁发生吸氧腐蚀 |
| D. | 向某未知溶液中滴加酸性KMnO4溶液 | KMnO4溶液褪色 | 溶液中有Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com