
.������16�֣�Ϊ��֤�����ԣ�Cl2>Fe3+>SO2��ijС������ͼ��ʾװ�ý���ʵ�飨�г������ͼ��м���װ�����ԣ��������Ѽ��飩��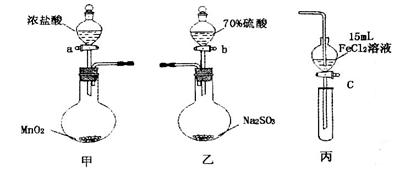
ʵ�鲽�裺
1.�ڼ�װ���У�����a�����ȣ���װ���г�������ɫ����ʱ�����װ�����ӡ�
2.����װ����FeC12��Һ���ʱ��ֹͣ���ȡ�
3.����c��ʹԼ2mL����Һ�����Թ��У�������Һ�е����ӡ�
4.����װ���У�����b���������ž������в���������ͨ��������װ�ñ�ƺ����Һ�У�һ��ʱ���ֹͣ��
5.���±����Թܣ�����c��ʹԼ2mL����Һ�����Թ��У�������Һ�е����ӡ�
�ش��������⣺
��1�����з�����Ӧ�Ļ�ѧ����ʽΪ___________________________________________��
��2����70%��������ȡSO2����Ӧ���ʱ���98%������죬ԭ����__________________��
��3��ʵ���У�֤��������Fe3+��SO2�����ӷ���ʽΪ_____________________________��
��4����I��II��III����ͬѧ�ֱ����������ʵ�飬ʵ�������£�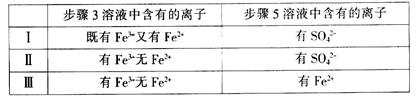
����ʵ����һ���ܹ�֤��������:Cl2>Fe3+>SO2����___________���á�I������II������III�����Żش𣩡�
��5����Ҫ�����ϼͱ�װ��֤��������Ϊ��Cl2> Fe3+> I2�Ľ��ۣ�����Ϊ��
��������©���м��������Լ�_________��_________��һ���ܼ�__________��
�ڽ���װ���в�����Cl2����ͨ����У��۲����©������Һ��ɫ�仯��
������۲쵽������Һ_______________________________________�������ȷ��
��ֹͣͨ��Cl2��
33.�𰸣�16�֣�
��1��MnO2 + 4 HCl��Ũ��= MnCl2 + Cl2��+ 2H2O �����ȣ���2�֣�����д�����ȡ�����Ũ�����÷֣�����������ſ�1�֣�
��2��70%��H2SO4��98%��H2SO4����̶ȴ���Һ��H+Ũ�ȴ�Ӧ�ٶȿ� ��2�֣���ֻ��70%��H2SO4��Һ��Һ��H+Ũ�ȴ�Ҳ�ɵ÷֣�
��3��2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO32- + 4H+��2�֣�
��4����͢� ��4�֣���2�֣�
��5����FeI2��KSCN��CCl4��3�֣�
���²㣨CCl4�㣩������ɫ��Ϊ�Ϻ�ɫ��1�֣������ϲ���Һ��dz��ɫ��1�֣���Ϊ��ɫ��1�֣���
������������� ��1�����ݼ�װ���е�������ʾ�������жϸ�װ����ʵ�����Ʊ������ķ���װ�ã����Ը�װ���з����ķ�Ӧ��MnO2 + 4 HCl��Ũ��= MnCl2 + Cl2��+ 2H2O��
��2��װ������ʵ�����Ʊ�SO2�ķ���װ�ã��÷�Ӧ��ԭ���������ѻӷ�������ǿ�������Ʊ����Խ������ֽ�������ᣬ����Ҫ�Ͽ��Ƶý϶�������ᣨSO2������Ҫ��Һ�к��е������ӵ�Ũ�Ƚϴ����Զ��ڲ�ͬŨ�ȵ�������ԣ������Ũ��С������̶�Խ��������70%��������ȡSO2����Һ��H+Ũ�ȴ�Ӧ���ʱ���98%������졣
��3������֤��������Fe3+��SO2 �����ڱ�Ƶ��Ȼ�������ͨ��SO2��SO2�ֱ�Fe3+ ���������Է�Ӧ�����ӷ���ʽΪ2Fe3+ + SO2 + 2H2O =" 2" Fe3+ + SO32- + 4H+ ��
��4��I��ͬѧ����õ��IJ���3��Һ�Ⱥ���Fe3+�ֺ���Fe2+ ��˵����Һ�е�Fe3+ �������������ã���һ�������й��������������Բ���5�м���SO42- ��Ҳһ������Fe3+ ����SO2���ã���˿��Եó�����������:Cl2>Fe3+>SO2 ��III��ͬѧ���IJ���3��Һֻ��Fe3+����Fe2+����˵����Һ�е�Fe3+ �������������ã�������5�м���Fe2+��Ҳ����˵����Һ��Fe2+ ��SO2��ԭFe3+ ���ã����Կ��Եó�������:Cl2>Fe3+>SO2 �Ľ��ۡ�II��ͬѧ���IJ���3��Һֻ��Fe3+����Fe2+����III��ͬѧ���ƣ���Һ�ж��п����ܽ��й�������������˲���5�м���SO42- ���п������ܽ������еĹ�����������SO2���ã����Բ���˵��������Fe3+>SO2 �����ѡI��III��
��5����Ҫ�����ϼͱ�װ��֤��������Ϊ��Cl2> Fe3+> I2�Ľ��ۣ������Ҫ�ڷ�Һ©���м��뺬��Fe2+ ��I-���Լ������Կ���ѡ��FeI2 ����Һ��֤������������Fe3+�� I2 ����Ҫ��������Ե��Լ�KSCN���л��ܼ���CCl4�����۲�ֲ����Һ���ϲ�dz��ɫ��죬�²����Ϻ�ɫ���������ȷ��
���㣺���⿼�����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������п��������������ã�������ҩ����ˮ���ȣ�4.74g����������[KAl(SO4)2��12H2O]������ˮ�Ĺ����е���������m~n(��Ʒ���������¶ȱ仯������)���¡�
��ش��������⣺
��1����ȷ��70��ʱ�������ʵĻ�ѧʽ____________________ (Ҫ��д���ƶϹ���)��
��2��д��200��ʱ������Ӧ�Ļ�ѧ����ʽ______________________________��
��3����770��ʱ������գ����õ��������A������B��B��ȫ���ܽ���BaCl2��Һ�в��γɰ�ɫ������A�ɲ�������ˮ�����˺�õ�����C����ҺD����D�м���BaCl2��ҺҲ�ܵõ���ɫ��������C����������NaOH��Һ��ǡ�÷�Ӧ�õ��������ҺE����n�й���ɷ��ǵ�_________�������ֱ�Ϊ__________B�Ļ�ѧʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ɷ����Ʊ�FeCl2����Ҫ�������£�
����ͼ��ʾ�����Ʊ�FeCl3?6H2O 
��1�����в�������ĵ���ʽ�� ��
��2�������ӷ���ʽ��ʾ���̢���ϡ��������� ���ڸù�����Ҫ��������Һ�в������ᣬĿ���� ��
����FeCl3 ? 6H2O�Ƶø���FeCl2�Ĺ������£�
������ʢ��FeCl3 ? 6H2O�������м���SOCl2�����ȣ������ˮFeCl3
��������ˮFeCl3���ڷ�Ӧ���У�ͨ����в���������һ��ʱ�����ȣ�����FeCl2
�����ռ�FeCl2�����汸��
��3�� SOCl2��ˮ�Ӵ���Ѹ�ٲ���������SO2�����ȷֽ�FeCl3 ? 6H2O���ܵõ���ˮFeCl3�������袡�пɵõ���ˮFeCl3����ϱ�Ҫ��ѧ����ʽ���͵õ���ˮFeCl3��ԭ�� ��
��4�����̢��в���FeCl2�Ļ�ѧ����ʽ�� ��
��FeCl2�İ�װ�����а�ȫע����������������£�
| Ʒ �� | �Ȼ����� |
| �������� | ��ɫ���������ױ�ɻ�ɫ������ˮ���и�ʴ�ԡ��� |
| ע������ | ����Ӵ���������ȣ�����ϩ����Ͱ��װ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������Ľ���֮һ��
��1��Ũ���ᡢŨ���������������������ԭ���� ��
��2����������ҪӦ���ڻ���ƽ�������ҵ��������ˮ�Ȼ������⻯��ﮣ�LiAlH4�����л��ܼ��з�Ӧ�Ƶ�����������ѧ����ʽ���£�3LiAlH4+AlCl3="4Al" + 3LiCl + 6H2��
�÷�Ӧ��������Ϊ ��
��3���⻯���ƣ�NaAlH4����һ����Ҫ�Ĵ�����ϣ���֪��
NaAlH4(s)=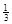 Na3AlH6 (s)+
Na3AlH6 (s)+ 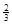 Al (s) + H2(g) ��H��+ 37 kJ��mol��1
Al (s) + H2(g) ��H��+ 37 kJ��mol��1
Na3AlH6(s)="3NaH(s)+" Al (s) + 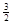 H2(g) ��H��+ 70.5 kJ��mol��1
H2(g) ��H��+ 70.5 kJ��mol��1
��NaAlH4(s)=" NaH(s)" + Al (s) +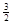 H2(g) ��H�� ��
H2(g) ��H�� ��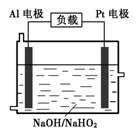
��4����֪H2O2��һ�����ᣬ��ǿ������Һ����Ҫ��HO2����ʽ ���ڡ�Ŀǰ�о��Ƚ����ŵ�Al��H2O2ȼ�ϵ�أ���ԭ������ͼ��ʾ������ܷ�Ӧ���£�
2Al+3HO2��+3H2O =2[Al(OH) 4]��+OH��
��������ӦʽΪ ��
������ͨп�̸ɵ����ȣ���������ͬ�����ĸ�����������ʱ��Al��H2O2ȼ�ϵ�ص����۷ŵ���ԼΪ��ͨп�̸ɵ�ص�______����
��Al�缫�ױ�NaOH��Һ��ѧ��ʴ�����Ǹõ��Ŀǰδ���ƹ�ʹ�õ�ԭ��֮һ����Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��14�֣�����A�����ڹ�ҵ���������ᣬ�����ʼ�ת������ͼ������CΪ����ɫ��
ĩ��DΪ��ʹƷ����Һ��ɫ����ɫ���塣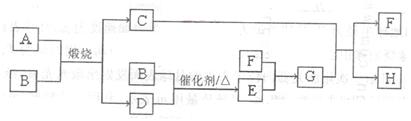
��ش�
��1��F�ĵ���ʽΪ_________��
��2�����������C��D��������Ϊ5:8����A�Ļ�ѧʽΪ______________��
��3����Dͨ��H��Һ�з�����Ӧ�����ӷ���ʽΪ_____________��
��4�����ʵ���Ũ�Ⱦ�Ϊ0.lmol/L��G��H�Ļ����Һ�У�����Ũ���ɴ�С��˳��
Ϊ____________��
��5�������õ��ij������Һ�ķ���ͬʱ�Ʊ�G��Ũ��Һ��Ũ����������Һ����ͼ��
ʾ����
��a��Ϊ��Դ��_________�������������������
��N���ռ�������Ϊ__________���ѧʽ����ͬ������
Q���ռ���Ϊ_________Ũ��Һ��
��ij���ʵı�����Һ���ѡ��___________�����Լ����ƣ���
�������ĵ缫��ӦʽΪ____________��
��6������H�н��������ӵķ���___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��ҵ���Ի�ͭ����Ҫ�ɷ�CuFeS2��Ϊԭ���Ʊ�����ͭ�����������ֹ��ա�
I.���������գ����������Ļ�ͭ�����ʯӢ����ͨ�˿������б��գ������Ƶô�ͭ��
��1�����յ��ܷ�Ӧʽ�ɱ�ʾΪ2CuFeS2+ 2SiO2+5O2��2Cu+2FeSiO3+4SO2�÷�Ӧ���������� ��
��2�����д���SO2�ķ���������������_____
A�߿��ŷ� B�ô�����Һ�����Ʊ���������
C�ð�ˮ���պ��پ������Ʊ������ D��BaCl2��Һ�����Ʊ�BaSO3
��3��¯����Ҫ�ɷ���FeO��Fe2O3��SiO2��Al2O3�ȣ�Ϊ�õ�Fe2O3�������ܽ�������������У�δ�漰���IJ����� ��
A���� B�ӹ���NaOH��Һ C�����ᾧ D���� E��������
II. FeCl3��Һ��ȡ������������������ͼ��ʾ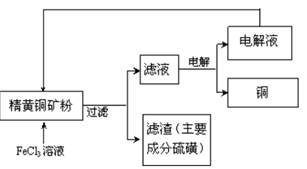
��4�����������У�CuFeS2��FeCl3��Һ��Ӧ�����ӷ���ʽΪ_____________��
��5���ù��������У�����ѭ�����õ������� ���ѧʽ����
��6������ʯī�缫�����Һ��д�������ĵ缫��ʽ_____________��
��7����ͭ���к�����Pb������C1һŨ�ȿɿ�����Һ��Pb2+��Ũ�ȣ���c(C1һ)��2mo1��L-1ʱ����Һ��Pb2+���ʵ���Ũ��Ϊ mol��L-1��[��֪KSP(PbCl2)��1 x 10һ5]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
ʵ���Ҳ���MgCl2��AlCl3�Ļ����Һ�������ˮ��Ӧ�Ʊ�MgAl2O4����Ҫ��������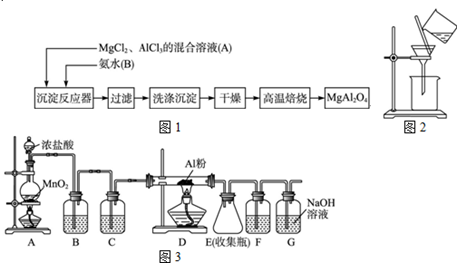
��1��ΪʹMg2+��Al3+ͬʱ���ɳ�����Ӧ���������Ӧ���м��� ���A����B�����ٵμ���һ��Ӧ��Ʊ�MgAl2O4�����У����±���ʱ������Ӧ�Ļ�ѧ����ʽ ��
��2������ͼ��ʾ�����˲����е�һ�������� ��
��3���ж������г����Ƿ�ϴ�����õ��Լ��� �����±���ʱ������ʢ�Ź�������������� ��
��4����ˮAlCl3��183������������ʪ��������������������ʵ���ҿ�������װ���Ʊ���װ��B��ʢ�ű���NaCl��Һ����װ�õ���Ҫ������ ��F���Լ��������� ����һ������װ���ʵ��Լ���Ҳ����F��G�����ã���װ����Լ�Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
���ǻ��õļ����Ԫ�أ��Ƽ��仯�������������������й㷺��Ӧ�á�
������м��㣺
��1���������ƣ�NaN3����ײ���ֽ�����ƺ͵������ʿ�Ӧ����������ȫ���ҡ���78�˵���������ȫ�ֽ⣬������״���µ���___________________L ��
��2����-�غϽ���ں˷�Ӧ���������Ƚ���Һ��5.05 g��-�غϽ�����200 mLˮ����0.075 mol������������Һ���������Ƶ����ʵ���Ũ��______________________������Һ������仯����
��3������������Һ�����������ˣ��õ��������Ƶ���Һ�������Һ��ͨ�������̼�������з�Ӧ�� 2NaAl(OH)4+CO2��2Al(OH)3��+Na2CO3+H2O����֪ͨ�������̼112 L����״���£������ɵ�Al(OH)3��Na2CO3�����ʵ���֮��Ϊ4:5���������Һ��ͨ��Ķ�����̼Ϊ224L����״���£����������ɵ� Al(OH)3��Na2CO3�����ʵ��������ֵ��
��4��Ϊ�ⶨij�������պ�������������������е�Ԫ�ص������������ֽ���ͬ��������ι���ֱ���뵽50.00mL��ͬŨ�ȵ�����������Һ�У���ˮԡ����������ȫ���ݳ�(���¶�����β��ֽ�)�������徭�������Ũ����������ȫ���ⶨŨ�������ӵ����������ֲⶨ������±���
| ������/g | 10.00 | 20.00 | 30.00 | 50.00 |
| Ũ�������ӵ�����/g | m | m | 1.29 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
һ��ⶨ��Ʒ�гɷֺ�����ʵ��Ӧ�ظ�2��3�Ρ�Ϊ�˲ⶨij�������ƹ����л��е�̼
���Ƶ������������ס��ҡ�����λͬѧ�ֱ����������ʵ�鷽����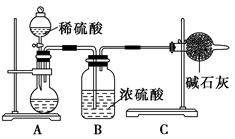
��.��ͬѧ�ķ�����ͼ��ʾ��
(1)��μ���Aװ�õ������ԣ�___________________________________��
(2)��ͬѧ�ظ�����������ʵ�飬�õ�̼���Ƶ��������������ݴ��ڽϴ��ƫ�����Ϊ��������������ƫ�͵�ԭ����________(�����)��
A��װ����ԭ�п����еĶ�����̼����Ҳ����ʯ������
B��װ��������е�ˮ�����Ͷ�����̼����ʯ������
C����Ӧ��ɺ�װ���еĶ�����̼û��ȫ������ʯ������
D������ϡ����������㡢��Ӧ�����
(3)Ϊ���ü�ʵ����������ȷ��������ʵ�鲽�趼��ȷ�������£�����Ϊͼ�е�ʵ��װ��Ӧ����θĽ���___________________________________________��
��.��ͬѧ�ķ����ǣ���ͼ�����ṩ��װ����ѡ��ʵ��װ�ã������ͬѧʵ��װ���е�B��C��ͨ���ⶨ�ų��Ķ�����̼�����(�����Ƕ�����̼����ˮ)�����㡣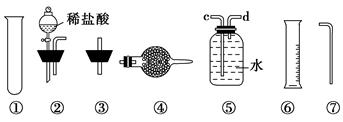
ѡ�����װ�õ�����˳��Ϊ________��
��.��ͬѧ�ķ����ǣ���ȡ��Ʒm g�����ܽ⣬��������Ȼ�����Һ�����ˡ�ϴ�ӡ���ɡ��������ù���n g��
(1)����100 mL 0.10 mol/L BaCl2��Һ��ʵ��������IJ����������ձ�������������ͷ�ιܡ���Ͳ���______(����������)��
(2)�������̼���Ƶ���������Ϊ(��m��n��ʾ)________��
(3)Ca2����Ba2��������ʹCO32��������ȫ���ܷ�ʹ���Ȼ�����Һ�����Ȼ�����Һ��________(��ܡ���)��ԭ���ǣ�______________________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com