
| A、甲烷可与水形成氢键这种化学键 |
| B、乙醇与水互溶可以用相似相溶原理解释 |
| C、H2O的熔点沸点大于H2S的是由于H2O分子之间存在氢键 |
| D、HF、HCl、HBr、HI的熔点沸点升高与范德华力大小有关 |


科目:高中化学 来源: 题型:
| A、氯离子全部参加了反应 |
| B、氟离子只有一部分参加反应 |
| C、氟化银难溶于水 |
| D、氟化钠和硝酸银在溶液中无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用托盘天平称取3.23gNaCl固体 |
| B、用10mL量筒量取7.50mL稀盐酸 |
| C、分液以后下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
| D、稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO中氯元素的化合价为-1价 |
| B、NaClO是一种钠盐 |
| C、Na、Cl、O由三种元素组成 |
| D、NaClO中Na、Cl、O的原子个数比为1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
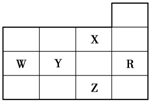
| A、其气态氢化物的稳定性是X>Y>W>Z |
| B、其最高价氧化物对应的水化物的酸性:Y>W |
| C、电负性、第一电离能的大小顺序都是X>Y>W |
| D、Y、Z的阴离子电子层结构都与R原子的相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酒精灯在桌子上倾倒着火,立即用湿布盖灭 |
| B、大量有毒、易燃气体在室内扩散,立即打开排风扇开关 |
| C、少量碱液沾到皮肤上,应立即用大量水冲洗 |
| D、配制硫酸时,可先在烧杯章加入一定体积的水,再在搅拌条件下,慢慢加入浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2 |
| B、Cl2O |
| C、ClO2 |
| D、Cl2O3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com