


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L甲酸溶液的c(H+)=10-2mol/L |
| B、甲酸以任何比与水互溶 |
| C、10mL1mol/L甲酸恰好与10mL1mol/LNaOH溶液完全反应 |
| D、甲酸溶液的导电性比盐酸溶液弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu能与浓硝酸反应,而不与浓盐酸反应 |
| B、Cu与浓硝酸反应比与稀硝酸反应快 |
| C、N2与O2在常温、常压下不反应,放电时可反应 |
| D、Fe与浓盐酸反应快,与稀盐酸反应慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 |
| B、液氨汽化时要吸收大量的热,可用作制冷剂 |
| C、生石灰能与水反应,可用来干燥氯气 |
| D、氯化铝是一种电解质,可用于电解法制铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
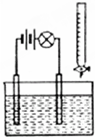 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A、向盐酸中逐滴加入食盐溶液 |
| B、向硫酸溶液中逐滴加入氢氧化钠溶液 |
| C、向硫酸溶液中逐滴加入氢氧化钡溶液 |
| D、向醋酸溶液中逐滴加入氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com