
(18分)下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 | 发生装置 |
① | 制氧气 | H2O2―→O2 | |
② | 制氨气 | NH4Cl―→NH3 | |
③ | 制氯气 | HCl―→Cl2 |
(1)上述实验原理中,从反应中有无电子转移的角度看,明显不同于其他气体的是 (填编号),写出实验室常用的制取该气体的化学方程式:______________________________________。
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其字母填入上表的空格中。
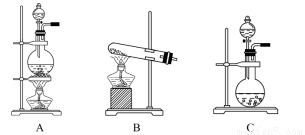
(3)若用上述制备O2的装置制备NH3,应选择的试剂为 。
(4)在浓CaCl2溶液中通入NH3和CO2可以制得碳酸钙,制取时应先通入的气体是 ,该反应的化学方程式为:____________________________________________________。
(5)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制。
①需要用量筒量取12 mol·L-1的盐酸的体积为 mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为 。
A.100 mL量筒
B.托盘天平
C.玻璃棒
D.50 mL容量瓶
E.10 mL量筒
F.胶头滴管
G.100 mL烧杯
H.100 mL容量瓶
③下列实验操作中不正确的是 (填写字母)。
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2 cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次
(18分) (1) ②(2分) Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O (2分)
CaCl2+2NH3↑+2H2O (2分)
(2)①C ②B ③A或C (各1分)
(3)浓氨水、NaOH或生石灰 (2分)
(4)NH3 (1分) CaCl2+CO2+2NH3+H2O===CaCO3↓+2NH4Cl (2分)
(5)①66.7 ②ACFGH ③B、C (各2分)
【解析】
试题分析:(1) ①制氧气③制氯气是氧化还原反应,②制氨气是复分解反应;(2) ①制氧气是液体与固体混合不加热制气体应选装置C,②制氨气是加热固体混合物制气体应选装置B,③制氯气是加热液体与固体混合物制气体应选装置A;(3) 若选择液体与固体混合不加热制氨气,就选择浓氨水与生石灰或氢氧化钠固体制备氨气;(4) NH3在水中的溶解度较大,CO2在水中的溶解度较小,应先通入NH3 ,反应方程式为CaCl2+CO2+2NH3+H2O===CaCO3↓+2NH4Cl ;(5) ①由稀释定律,需要盐酸的体积为8 mol·L-1×100 mL÷12 mol·L-1=66.7 mL;②为完成配制需要选择的仪器为A.100 mL量筒 C.玻璃棒 F.胶头滴管 G.100 mL烧杯 H.100 mL容量瓶;③A、使用容量瓶前,检查它是否漏水,A正确;B、容量瓶用蒸馏水洗净后,不能用待配溶液润洗,润洗后所配溶液浓度偏高,B错误;C、浓盐酸应在烧杯中稀释,不能在容量瓶中稀释,C错误;D、定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次,D正确;答案选BC。
考点:化学实验操作、气体的制备、一定物质的量浓度溶液的配制


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年河南省高三12月月考理综化学试卷(解析版) 题型:选择题
含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子或物质沉淀pH见下表)
离子 | Mg2+ | Al 3+ | 物质 | Al(OH)3 |
开始沉淀pH | 8.93 | 3.56 | 开始溶解pH | 8.04 |
完全沉淀pH | 10.92 | 4.89 | 完全溶解pH | 12.04 |

查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邢台市高三上学期第四次月考化学试卷(解析版) 题型:选择题
X、Y、Z、W是短周期元素,原子序数依次递增。X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14。下列说法正确的是
A.气态氢化物的稳定性:X<Z <W
B.Y的阳离子半径比W的阴离子半径小
C.X、Z、W氧化物对应水化物酸性的强弱顺序为X<Z< W
D.室温下,含Y元素的盐形成的水溶液其pH<7
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邢台市高三上学期第四次月考化学试卷(解析版) 题型:选择题
下列电子式书写正确的是
A.溴化铵: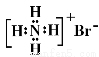
B.硫化氢: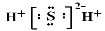
C.氮气:
D.羟基: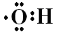
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
已知反应方程式:NH4NO3+Zn=ZnO+N2↑+2H2O,下列有关说法中正确的是
A.该反应中NH4NO3只作氧化剂 B.ZnO是还原产物
C.氧化产物只有N2 D.该反应每生成1mol N2转移5mol电子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列有关物质的性质和应用的说法中正确的是
A.SiO2既能溶于NaOH溶液又能溶于氢氟酸,说明SiO2是两性氧化物
B.浓硫酸能干燥SO2等气体,说明浓硫酸具有吸水性
C.SO2气体具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D.自来水厂可用明矾对水进行消毒杀菌
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市高三上学期期中考试化学试卷(解析版) 题型:填空题
已知KCl、K2Cr2O7、CrCl3、Cl2 、HCl在溶液中可以形成一个氧化还原反应体系。
(1)已知反应中有水生成,则反应物分别是K2Cr2O7和 (填化学式),当电子转移数为6mol时,化学方程式中水的化学计量数是 。
(2)反应过程中,被还原的元素是_________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高一上学期期中考试化学试卷(解析版) 题型:填空题
(10分)小美在五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。请完成下列问题:
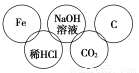
(1)五连环中发生的反应中
①属于置换反应的化学方程式为_________________________________________________;
②属于复分解反应的化学方程式为_________________________________________________;
③属于化合反应的化学方程式为__________________________________________________________。
(2)写出CO2与NaOH溶液反应的化学方程式_____________________________________________________。
(3)上述反应中属于氧化还原反应的有________个。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com