
| A. | 盐酸 | B. | KSCN溶液 | C. | 氨水 | D. | 烧碱溶液 |
分析 七种溶液含有的阳离子各不相同,但都是氯化物,因而KSCN溶液不能达到目的,且盐酸与七种氯化物都不反应,利用金属氢氧化物的溶解性及颜色来鉴别,因又涉及到Al3+和Mg2+的鉴别,因此必需选强碱.
解答 解:A.加入盐酸,与七种物质都不反应,不能鉴别,故A错误;
B.加入KSCN只能鉴别FeCl3,不能鉴别其它物质,故B错误;
C.加入氨水,不能鉴别MgCl2、AlCl3,故C错误;
D.加入氢氧化钠,NaCl无现象,FeCl2生成白色沉淀,然后迅速变成灰绿色,最后变成红褐色,FeCl3生成红褐色沉淀,AlCl3先生成白色沉淀,沉淀然后溶解,MgCl2生成白色沉淀,CuCl2生成蓝色沉淀,NH4Cl有刺激性气体生成,现象各不相同,可鉴别,故D正确.
故选D.
点评 本题考查物质的检验和鉴别,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关物质的性质,题目难度不大.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 在NaHS溶液中滴人少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大,pH增大 | |
| B. | 常温下,由于HCO3-水解显碱性,所以饱和NaHCO3溶液显碱性 | |
| C. | 泡沫灭火器是利用Al2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 | |
| D. | 配制氯化铝溶液时,先将氯化铝溶于浓硫酸,再加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
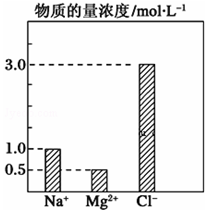 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中可能存在Mg2+和Fe3+ | B. | 溶液中可能存在Br-和Cl- | ||
| C. | 溶液可能存在Ba2+和Cl- | D. | 溶液中一定存在Na+和CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HNO3═H++N5++3O2- | B. | Ca(OH)2═Ca2++(OH-)2 | ||
| C. | AlCl3═Al+3+3Cl- | D. | Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com