
【题目】高铁酸钾(![]() )是新型的绿色环保水处理剂。一种制备
)是新型的绿色环保水处理剂。一种制备![]() 的流程如下:
的流程如下:
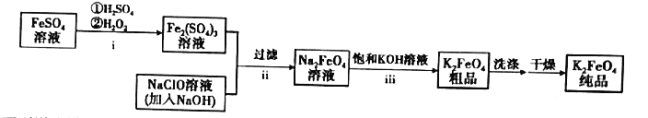
下列说法错误的是( )
A.步骤i中反应的离子方程式为![]()
B.步骤ⅱ说明碱性条件下,氧化性:![]()
C.步骤ⅲ的反应为复分解反应,说明溶解度:![]()
D.![]() 作为性能优良的水处理剂,主要是利用了其强氧化性和还原后产生的具有絮凝作用的Fe(Ⅲ)
作为性能优良的水处理剂,主要是利用了其强氧化性和还原后产生的具有絮凝作用的Fe(Ⅲ)
【答案】BC
【解析】
根据制备流程分析,FeSO4溶液在酸性条件下与H2O2发生氧化还原反应得到Fe2(SO4)3,Fe2(SO4)3与NaClO在碱性条件下发生氧化还原得到Na2FeO4,Na2FeO4与饱和的KOH溶液得到K2FeO4粗品,经洗涤干燥后得到K2FeO4纯品,据此分析解答问题。
A.由上述分析可知,步骤ⅰ为FeSO4溶液在酸性条件下与H2O2发生氧化还原反应生成H2O和Fe2(SO4)3,根据氧化还原反应规律可得反应的离子方程式为:2Fe2++H2O2+2H+===2Fe3++2H2O,A选项正确;
B.步骤ⅱ为Fe2(SO4)3与NaClO在碱性条件下发生氧化还原得到Na2FeO4,氧化剂是NaClO,氧化产物为Na2FeO4,因为氧化剂的氧化性大于氧化产物,故氧化性:NaClO>Na2FeO4,B选项错误;
C.步骤ⅲ为Na2FeO4与饱和的KOH溶液发生复分解反应得到K2FeO4粗品,溶解度大的物质转化为溶解度小的物质,故溶解度:Na2FeO4>K2FeO4,C选项错误;
D.由于K2FeO4具有强氧化性,因此可用于水的杀菌消毒,且其还原产物产生的Fe3+水解得到Fe(OH)3的胶体,具有絮凝的作用,故K2FeO4是乙中性能优良的水处理剂,D选项正确;
答案选BC。


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:
【题目】某有机化合物A对氢气的相对密度为30,分子中含碳40%,含氢6.6%,其余为氧。
(1)通过计算确定该有机物的分子式;____
(2)按中学常见官能团,写出其可能的结构简式。____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。抗击疫情要戴口罩,勤洗手,下列有关说法正确的是( )
A.新型冠状病毒可能通过气溶胶传播,说明病毒的粒子直径可能在纳米级范围内
B.为增强消毒效果可将医用消毒酒精与84消毒液混合使用
C.甲醛和戊二醛可杀灭多种病原体,可用于空气、餐具的消毒
D.可用铝制容器配制过氧乙酸(![]() )消毒剂
)消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案的设计能达到相应实验目的的是( )
选项 | 实验目的 | 实验方案 |
A | 验证 | 向 |
B | 比较HF与 | 常温下,用pH试纸分别测定浓度均为 |
C | 验证 | 向 |
D | 比较Fe与Cu的金属活动性 | 常温下,将Fe、Cu与浓硝酸组成原电池 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应X2+3Y2![]() 2Z2在反应过程中,反应速率(v)与时间(t)的关系曲线如图所示,下列叙述正确的是
2Z2在反应过程中,反应速率(v)与时间(t)的关系曲线如图所示,下列叙述正确的是
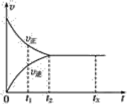
A.t1时,只有正方向反应
B.t2时,反应未达到限度
C.t2~t3,正、逆反应速率相等
D.t2~t3,各物质的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
Fe3O4(s)+4H2(g)在温度和容积不变的条件下进行。能表明反应达到平衡状态的叙述是
A. Fe3O4的物质的量不变 B. V(H2O)=V(H2)
C. 反应不再进行 D. 容器内压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。
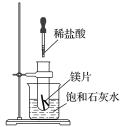
回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)写出有关反应的离子方程式____________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表中的一部分,回答下列问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ | ⑾ | ⑿ |
(1)写出下列元素名称①_______,⑤_______,⑨_______,⑾________。
(2)在这些元素中,金属性最强的元素是_______;除稀有气体元素以外的元素中原子半径最大的是_______,原子半径最小的是______。其氢化物最稳定的是____。(填写元素符号)
(3)元素②和③形成的离子的电子层结构_________(填“相同”或“不相同”),两者形成的化合物是否是离子化合物________(填“是”或否”),该化合物的电子式为______________。
(4)元素⑧的最高价氧化物对应的水化物化学式为:______名称为______:。
(5)在这些元素的最高价氧化物对应的水化物中,属于两性氢氧化物的是_________(填写化学式),写出其和盐酸反应的化学方程式__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com