
����Ŀ������β���dz�����Ҫ������Ⱦ�������ȼ������ʱ������Ӧ��N2(g) + O2(g)![]() 2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��
2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��
��1����֪H2��CO���Դ���ԭNO�Դﵽ������Ⱦ��Ŀ�ġ�N2(g) + O2(g) = 2NO(g) ��H= +180.5 kJ��mol-1,2H2(g) + O2(g) = 2H2O(l) ��H=��571.6 kJ��mol-1,��H2(g)��NO(g)��Ӧ����N2(g)��H2O(l)���Ȼ�ѧ����ʽ��_________________________,�жϸ÷�Ӧ�Է����е�������_______________��������Է��������Է�������
��2��������һ��ʱ�������������ı���������ѧ��Ӧ���ʡ���ͼ��ʾ��������������ʱ����Ӧ��2NO(g) + 2CO(g)![]() 2CO2(g) + N2(g)��NO��Ũ��[c(NO)]���¶ȣ�T���������������S����ʱ�䣨t���ı仯���ߡ�
2CO2(g) + N2(g)��NO��Ũ��[c(NO)]���¶ȣ�T���������������S����ʱ�䣨t���ı仯���ߡ�

����÷�Ӧ�ġ�H___0���������������
���������ı����S1��S2 ���ڸ�ͼ�л���c(NO)��T1��S2�����´ﵽƽ������еı仯����___��
��3��ijС����һ���º�ѹ��������9mol N2��23mol H2ģ��ϳɰ���Ӧ��ͼCΪ��ͬ�¶���ƽ�������а����������������ѹǿ��p���Ĺ�ϵͼ������ϵ��T2��60MPa�´ﵽƽ�⣮

�����ж�N2��g��+3H2��g��2NH3��g���ﵽƽ�����___������ţ���
a��������ѹǿ���ٷ����仯 b�����������ܶȲ��ٷ����仯
c��v����N2��=3v����H2�� d����������ƽ����Է����������ٷ����仯
�ڴ�ʱN2��ƽ���ѹΪ_________MPa������ѹ=��ѹ�����ʵ������������������ʱ��ƽ�ⳣ��Kp=__________����ƽ���ѹ����ƽ��Ũ�ȼ��㣬�������2λ��Ч���֣���
���𰸡�2H2(g) + 2NO(g) = N2(g) + 2H2O(l) ��H=��752.1 kJ��mol-1 �����Է� ��  bd 9 0.043
bd 9 0.043
��������
��1�����ݸ�˹���ɣ�����֪�Ȼ�ѧ����ʽ�����ʵ���ϵ�����мӼ�����Ŀ���Ȼ�ѧ����ʽ����Ӧ��Ҳ������Ӧ��ϵ��������Ӧ�ļ��㣻�����Է���Ӧ���е��жϹ�ʽ�жϣ�
��2���ٸ��ݵ���ƽ���ʱ�䣬�ж��¶ȸߵͣ��ٸ��ݲ�ͬ�¶��µ���ƽ��ʱNO��Ũ�ȸߵͣ��ж��¶ȶ�ƽ���Ӱ�죬�ݴ��жϷ�Ӧ��ЧӦ��
�ڴ����ı����S1��S2�������S1����ƽ���ʱ��ȴ���S2�̣�������Ӱ��ƽ���ƶ���ƽ��ʱNO��Ũ����ͬ���ݴ���ͼ��
��3���ٿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȡ��ٷֺ����Լ��ɴ������һϵ�����������䣻
���������η�����ʼ �仯 ƽ�⡱�г���������ݣ��ȼ�������ƽ���ѹ���ټ���ƽ�ⳣ��Kp��
��1����֪����N2��g��+O2��g��=2NO��g����H=+180.5kJ/mol����2H2��g��+O2��g��=2H2O��l����H=-571.6 kJmol-1�����ݸ�˹���ɿ�֪��-�ٵã�2H2��g��+2NO��g��=N2��g��+2H2O��l����H����H=��-571.6kJ/mol��-180.5kJ/mol�T-752.1kJ/mol����������Ӧ���ȣ���H��0����������Ӧ�������������С��Ϊ�ؼ�С�ķ�����S��0����H-T��S��0����Ӧ�Է����У�����T��С�ſ��ԣ����������Է����ʴ�Ϊ��2H2��g��+2NO��g��=N2��g��+2H2O��l����H=-752.1kJ/mol�������Է���
��2�����¶�T2����ƽ���ʱ��̣���Ӧ���ʿ죬���¶�T2��T1���¶�Խ�ߣ�ƽ��ʱNO��Ũ��Խ�ߣ�˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H��0���ʴ�Ϊ������
�ڴ����ı����S1��S2�������S1����ƽ���ʱ��ȴ���S2�̣�������Ӱ��ƽ���ƶ���ƽ��ʱNO��Ũ����ͬ����c��NO����T1��S2�����´ﵽƽ������еı仯����Ϊ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3����a���÷�Ӧ�Ǻ�ѹ���������۷�Ӧ�Ƿ�ﵽƽ��״̬ѹǿ�����䣬���Բ��ܾݴ��ж�ƽ��״̬����a����
b����Ӧǰ���������������䵫��������ı䣬���Ի��������ܶȸı䣬����������ܶȲ���ʱ�÷�Ӧ�ﵽƽ��״̬����b��ȷ��
c��3v����N2��=v����H2��ʱ�÷�Ӧ�ﵽƽ��״̬����v����N2��=3v����H2��ʱ�÷�Ӧû�дﵽƽ��״̬����c����
d����Ӧǰ���������������䣬�����������ʵ�����С�����Ի��������Է����������ӣ�����������ƽ����Է����������ٷ����仯ʱ�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����d��ȷ����ѡbd��
������ϵ��T2��60MPa�´ﵽƽ�⣬��ͬ�¶��£����������������������ʵ�����������ƽ��ʱn��NH3��=xmol��
N2��g��+3H2��g��![]() 2NH3��g��
2NH3��g��
��ʼ��mol�� 9 23 0
��Ӧ��mol�� 0.5x 1.5x x
ƽ�⣨mol�� 9-0.5x 23-1.5x x
ƽ��ʱ�����������=x/(32-x)=0.6,���x=12����N2��ƽ���ѹΪ![]() ��60MPa=9 MPa�������ķ�ѹ=60%��60MPa=36MPa��������ѹ=60MPa-9MPa-36MPa=15MPa����ʱ��ƽ�ⳣ��Kp=��36MPa��2/9 MPa��(15MPa)3=0.043��MPa��-2���ʴ�Ϊ��9��0.043��MPa��-2��
��60MPa=9 MPa�������ķ�ѹ=60%��60MPa=36MPa��������ѹ=60MPa-9MPa-36MPa=15MPa����ʱ��ƽ�ⳣ��Kp=��36MPa��2/9 MPa��(15MPa)3=0.043��MPa��-2���ʴ�Ϊ��9��0.043��MPa��-2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������ҵIJ���Ϊͭо�����������������յĵ��ԭ�������жϳ������������ʱͭо��( )
A.����B.����C.����D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ա���HCHO(��ȩ����O2���ǻ���ʯ��HAP)���������H2O�����̣�������ʾ��ͼ���£�ͼ��ֻ������ HAP�IJ��ֽṹ����
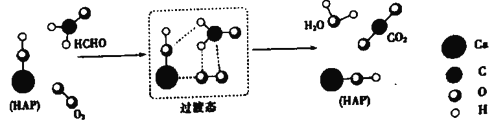
����˵������ȷ����
A. HAP�����HCHO��O2�ķ�Ӧ����
B. HCHO�ڷ�Ӧ�����У���C-H����������
C. ����ͼʾ��Ϣ��CO2�����е���ԭ��ȫ������O2
D. �÷�Ӧ�ɱ�ʾΪ��HCHO+O2![]() CO2+H2O
CO2+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ں��º�ѹ�ܱ�����M����ͼ�ͺ��º����ܱ�����N����ͼ���У��������о�����a molA��a molB����ʼʱ�����������ΪVL���������·�Ӧ���ﵽ��ѧƽ��״̬��2A��?��+ B��?��![]() xC��g�� ��H��0��ƽ��ʱM��A��B��C�����ʵ���֮��Ϊ1��3��4�������жϲ���ȷ����
xC��g�� ��H��0��ƽ��ʱM��A��B��C�����ʵ���֮��Ϊ1��3��4�������жϲ���ȷ����

A. x��2
B. ��N��������ܶ���ͼ����ʾ����A��Bֻ��һ������̬
C. AΪ���壬BΪ�����壬��ƽ��ʱM��N��C�����ʵ������
D. ��A��B��Ϊ���壬ƽ��ʱM��A��ת����С��N��A��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ��ӦA(g����3B(g��![]() 2C(g����2D(g���������ֲ�ͬ������ò�ͬ���ʱ�ʾ�ķ�Ӧ����
2C(g����2D(g���������ֲ�ͬ������ò�ͬ���ʱ�ʾ�ķ�Ӧ����
�ֱ����£����з�Ӧ������������ ��
A��v(C����0.04 mol/(L��s��
B��v(B����0.06 mol/(L��min��
C��v(A����0.15 mol/(L��min��
D��v(D����0.01 mol/(L��s��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Դ����Ǧ���أ���ط�Ӧ���£� PbO2 + Pb + 2H2SO4 ![]() 2PbSO4+ 2H2O�����ݴ˷�Ӧ�ж�������������ȷ����(����)
2PbSO4+ 2H2O�����ݴ˷�Ӧ�ж�������������ȷ����(����)
A. PbO2�ŵ�ʱ�ǵ�صĸ��������ʱ�ǵ�ص�����
B. �����ĵ缫��ӦʽΪ��Pb + SO42���C 2e�C=PbSO4
C. �ŵ�ʱ��PbO2�õ��ӣ�������
D. ��طŵ�ʱ����Һ������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ij��Ӧ�ﵽƽ�⣬ƽ�ⳣ��K��c(CO)c(H2O)/c(CO2)c(H2)������ʱ���¶����ߣ�H2Ũ�ȼ�С������˵����ȷ����
A. �÷�Ӧ��ѧ����ʽΪCO��H2O ![]() CO2��H2 B. �����¶ȣ��淴Ӧ���ʼ�С
CO2��H2 B. �����¶ȣ��淴Ӧ���ʼ�С
C. ���º����£�����ѹǿ��H2Ũ��һ����С D. �÷�Ӧ���ʱ�Ϊ��ֵ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ����ɫ��ĩ����BaCl2��K2SO4��CaCO3��NaOH��CuSO4�е�һ�ֻ�����ɣ�Ϊ��̽�����ijɷݣ�����������ʵ�飺�����ж���ȷ���ǣ�������

A. BaCl2��CaCO3һ�����ڣ�NaOH���ܴ���
B. K2SO4��CuSO4һ��������
C. K2SO4��NaOH��CaCO3��BaCl2һ�����ڣ�CuSO4���ܴ���
D. CΪ��һ������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2H2(g)��O2(g)=2H2O(l) ��H����569.6kJ/mol,2H2O(g)=2H2(g)��O2(g) ��H����482.1 kJ/mol������1gҺ̬H2O������ʱ���յ������� (����)
A. 2.43 kJ B. 4.86 kJ C. 43.8 kJ D. 87.5 kJ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com