
某课外活动小组使用下列用品设计原电池。用品:铜片、铁片、导线、金属夹、发光二极管、果汁(橙汁、苹果汁)500mL,、烧杯。下列说法正确的是
A.该装置能将电能转化为化学能 B.实验过程中铜片逐渐溶解
C电子由铁片通过导线流向铜片 D.铁片上会析出红色的铜
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
某课外活动小组同学用如图Ⅰ装置进行实验,试回答下列问题。
图I 图II
(1)若开始时开关K与a连接,则B极的电极反应式为_____________。
(2)若开始时开关K与b连接,则总反应的离子方程式为_______ ______;
有关上述实验,下列说法正确的是(填序号)_____________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模仿工业上用离子交换膜法制烧碱的方法,设想用如图Ⅱ装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽工作时,通过阴离子交换膜的离子数_______(填“大于” “小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_____ ________。
(4)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s)4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为 kg。
查看答案和解析>>
科目:高中化学 来源:2011届广西桂林中学高三高考模拟试题(理综)化学部分 题型:实验题
某课外活动小组同学用如图Ⅰ装置进行实验,试回答下列问题。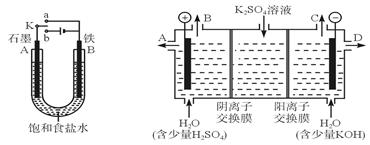
图I 图II
(1)若开始时开关K与a连接,则B极的电极反应式为_____________。
(2)若开始时开关K与b连接,则总反应的离子方程式为_______ ______;
有关上述实验,下列说法正确的是(填序号)_____________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模仿工业上用离子交换膜法制烧碱的方法,设想用如图Ⅱ装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽工作时,通过阴离子交换膜的离子数_______(填“大于” “小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_____ ________。
(4)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为 kg。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年广西桂林中学高三高考模拟试题(理综)化学部分 题型:实验题
某课外活动小组同学用如图Ⅰ装置进行实验,试回答下列问题。

图I 图II
(1)若开始时开关K与a连接,则B极的电极反应式为_____________。
(2)若开始时开关K与b连接,则总反应的离子方程式为_______ ______;
有关上述实验,下列说法正确的是(填序号)_____________。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(3)该小组同学模仿工业上用离子交换膜法制烧碱的方法,设想用如图Ⅱ装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽工作时,通过阴离子交换膜的离子数_______(填“大于” “小于”或“等于”)通过阳离子交换膜的离子数。
②通电开始后,阴极附近溶液pH会增大,请简述原因_____ ________。
(4)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为 kg。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题

 4SiHCl3(g),达到平衡后,H2与SiHCl3的物质的量浓度分别为0.140mol/L和0.020 mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为______kg。
4SiHCl3(g),达到平衡后,H2与SiHCl3的物质的量浓度分别为0.140mol/L和0.020 mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为______kg。 查看答案和解析>>
科目:高中化学 来源:0120 模拟题 题型:填空题

 4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为________kg。
4SiHCl3(g)达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于图Ⅱ离子交换膜法的电解产物,理论上需消耗硫酸钾质量为________kg。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com