
【题目】己知氨基酸可发生如下反应:
![]()
D、E的相对分子质量分别为162和144,可发生如下物质转化关系。如下图所示:

(1)写出B、D的结构简式:B________,D_________。
(2)写出C→E的化学方程式:_________________。
(3)写出C→D的化学方程式:_________________。
【答案】 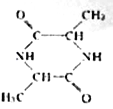
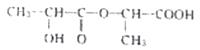

【解析】氨基酸能发生缩聚反应,脱去一个H2O分子,-COOH脱去-OH,-NH2脱去-H,发生缩聚反应生成蛋白质,由此可推知,结合B的分子式,两个丙氨酸分子间脱去2个H2O分子可生成B为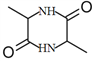 。由题目中所给信息可总结出:在HNO2作用下,氨基酸中的-NH2可转变成-OH,可得C:CH3CHOHCOOH。由于C中含有-COOH和-OH,发生脱水反应生成D与E,而D、E的相对分子质量分别为162和144,故C脱去一个水可得D为CH3CHOHCOOCH(CH3)COOH,C脱去两个水分子可得E为
。由题目中所给信息可总结出:在HNO2作用下,氨基酸中的-NH2可转变成-OH,可得C:CH3CHOHCOOH。由于C中含有-COOH和-OH,发生脱水反应生成D与E,而D、E的相对分子质量分别为162和144,故C脱去一个水可得D为CH3CHOHCOOCH(CH3)COOH,C脱去两个水分子可得E为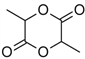 ,丙氨酸与氢氧化钠发生中和反应生成A为CH3CH(NH2)COONa,则
,丙氨酸与氢氧化钠发生中和反应生成A为CH3CH(NH2)COONa,则
(1)由上述分析可知,B的结构简式为 ,D的结构简式为CH3CHOHCOOCH(CH3)COOH;(2)C→E的化学方程式为2CH3CHOHCOOH
,D的结构简式为CH3CHOHCOOCH(CH3)COOH;(2)C→E的化学方程式为2CH3CHOHCOOH![]()
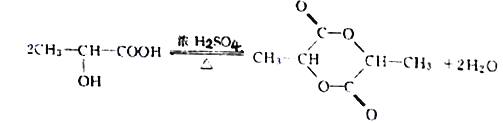
 +2H2O;(3)C→D的化学方程式为2CH3CHOHCOOH
+2H2O;(3)C→D的化学方程式为2CH3CHOHCOOH![]() CH3CHOHCOOCH(CH3)COOH+H2O。
CH3CHOHCOOCH(CH3)COOH+H2O。


科目:高中化学 来源: 题型:
【题目】下列有关细胞中化学元素及化合物的叙述,错误的是
A. 碳是各种有机化合物的最基本元素B. DNA和RNA的成分中都含有单糖
C. 性激素属于固醇类物质D. 胆固醇是各种生物细胞膜的重要成分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在元素周期表中,第三、四、五、六周期元素的数目分别是( )
A. 2.8, 8.18 B. 8.18.18.32 C. 8.18.18.18 D. 8.8.18.18
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题. 
(1)该浓盐酸中HCl的物质的量浓度为molL﹣1 .
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是 .
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl﹣的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次 并在操作步骤空白处填上适当仪器名称) .
A.用30mL水洗涤2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”,填B表示“偏小”,填C表示“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸钴[Cox(OH)y(CO3)z,相对分子质量为365]常用作电子材料、磁性材料的添加剂.碱式碳酸钴中的Co的化合价类似与Fe3O4中Fe的化合价,其中高价态具有强氧化性,而低价态在溶液中能稳定存在,受热时可分解生成三种氧化物。为了确定其组成,某化学兴趣小组同学设计了如图所示的装置进行实验:

(1)请完成下列实验步骤:
① 称取一定量的样品置于硬质玻璃管内,称量乙、丙装置的质量;
② 按如图所示装置组装好仪器,并_______________;
③ 加热甲中玻璃管,当乙装置中________(填实验现象),停止加热;
④ 打开活塞a,缓缓通入空气数分钟后,称量乙、丙装置的质量;
⑤ 计算。
(2)步骤④中缓缓通入空气数分钟的目的是____________。
(3)上述实验装置中存在一个明显缺陷。为解决这一问题,可在_____(填装置连接位置)增加一个_____装置(填字母)。
A.盛有浓硫酸的洗气瓶 B. 盛有无水氯化钙的U形管
C. 盛有P2O5的干燥管 D. 盛有碱石灰的干燥管
(4)若按正确装置进行实验,测得乙裝置增重0.36g,丙装置增重0.88g, 则该碱式碳酸钴的化学式为_________。
(5)该碱式碳酸钴与浓盐酸反应时,起酸性作用的HCl与被氧化的HC1的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述正确的是
A.构成原电池的正极和负极必须是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.在原电池中,电子流出的一极是负极,该电极被还原
D.原电池放电时,电流的方向是从负极到正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、 Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。

已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液
(1)稀酸A的分子式是_____________________。
(2)滤液1中加入H2O2溶液的目的是____________________。滤渣1中加入稀酸A和H2O2发生反应的离子方程是为______________________。
(3)某同学设计实验证明滤液1中含有Fe2+,他所用的试剂的化学式为______________。
(4)己知溶液中的Fe2+可以和难溶于水的FeO(OH)反应生成Fe3O4,请书写该反应的离子方程式__________。
(5)由滤液2生成Ce(OH)4的离子方程式_____________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,请用离子方程式解释其作用原理:_____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)有①质子数②中子数③核外电子数④价电子数⑤最外层电子数⑥电子层数。请用上述序号回答:
(1)原子种类由 决定,元素种类由 决定。
(2)原子的质量数由 决定,元素在周期表中的位置由 决定。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com