
| A.原子半径:C>D>A>B |
| B.原子序数:b>a>d>c |
| C.离子半径:D>C>A>B |
| D.单质还原性:A>B>C>D |
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素 | 熔点/℃ | 沸点/℃ | 与水的反应 | 导电性 |
| X | -209.9 | -195.8 | 不反应 | 不导电 |
| Y | -219.6 | -188.1 | 形成酸性溶液 | 不导电 |
| Z | 180.5 | 1347 | 形成碱性溶液 | 导电 |
| A.X、Y、Z | B.Z、X、Y | C.Y、X、Z | D.Z、Y、X |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ,并在世界上首次确认了β缓发裂变先驱核
,并在世界上首次确认了β缓发裂变先驱核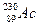 。根据以上信息完成下列问题:
。根据以上信息完成下列问题: 的中子数为_________________。
的中子数为_________________。 的中子数和电子数的差值为__________________。
的中子数和电子数的差值为__________________。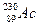 新核素的下列叙述正确的是___________。
新核素的下列叙述正确的是___________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Li<Na<K<Rb<Cs? |
| B.碱性:LiOH<NaOH<KOH<RbOH<CsOH? |
| C.熔沸点:Li<Na<K<Rb<Cs? |
| D.还原性:Li>Na>K>Rb>Cs |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③④⑤⑦⑧⑨ | B.③⑥⑦⑧ |
| C.③⑥⑦⑧⑨ | D.①②③④⑤⑥⑦⑧⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com