
| A. | Ca2+、K+、Cl-、NO3- | B. | Na+、Ca2+、SO32-、ClO- | ||
| C. | Al3+、K+、OH-、NO3- | D. | Na+、Ca2+、SiO32-、Cl- |
分析 酸溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:A.酸溶液中该组离子之间不反应,可大量共存,故A正确;
B.酸溶液中SO32-、ClO-发生氧化还原反应,不能大量共存,故B错误;
C.酸溶液中不能大量存在OH-,且OH-、Al3+结合生成沉淀,不能共存,故C错误;
D.酸溶液中不能大量存在SiO32-,且Ca2+、SiO32-结合生成沉淀不能共存,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 非金属元素的两原子之间不可能形成离子键 | |
| B. | 离子化合物不可能全部由非金属元素组成 | |
| C. | 含有非极性键的分子不一定是共价化合物 | |
| D. | 离子化合物中一定含有离子键. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
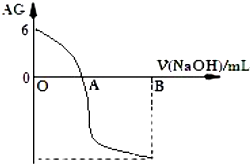
| A. | A 点时加入氢氧化钠溶液体积为 20 mL | |
| B. | OA 段溶液中:c(CH3COO-)>c(CH3COOH) | |
| C. | 室温时 0.01 mol/L的醋酸溶液 pH=4 | |
| D. | 若 B 点时加入 NaOH 溶液为 40 mL,所得溶液中:c(CH3COO-)+c(CH3COOH)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将0.2 mol/L的一元酸HA溶液和0.1 mol/L的NaOH溶液混合,混合液中一定有:c(OH-)+c(A-)=c(H+)+c(Na+) | |
| B. | 某溶液中由水电离出的c(OH-)=1×10-9mol/L,则该溶液的pH一定为5 | |
| C. | 室温下,NaHSO3溶液的pH<7,则溶液中c(SO32-)<c(H2SO3) | |
| D. | Na2CO3溶液与NaHCO3溶液混合一定有2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=+0.33 kJ•mol-1 | |
| B. | 单斜硫转化为正交硫的反应是吸热反应 | |
| C. | △H3<0,正交硫比单斜硫稳定 | |
| D. | △H3>0,单斜硫比正交硫稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于7.1g | B. | 小于7.1g | ||
| C. | 大于7.1g,小于14.2g | D. | 大于14.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
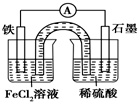
| A. | 原电池工作一段时间后,FeCl2溶液中c(Cl-)增大 | |
| B. | 此电池工作原理与硅太阳能电池工作原理相同 | |
| C. | Fe为正极,石墨上发生的反应为2H++2e-═H2↑ | |
| D. | 该装置中的盐桥完全可用金属导线代替 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
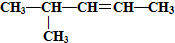
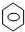 ⑥
⑥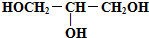 ⑦CH3CH2CH3
⑦CH3CH2CH3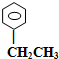 ⑨
⑨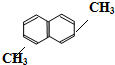 ⑩
⑩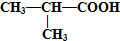
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com