
| A. | 氯气起杀菌消毒作用 | B. | 氯气氧化绿矾 | ||
| C. | 绿矾具有净水作用 | D. | 绿矾的氧化产物具有净水作用 |
分析 A.氯气与水反应生成次氯酸,次氯酸具有杀菌消毒作用;
B.绿矾中二价铁离子具有还原性,氯气能够氧化二价铁离子生成三价铁;
C.绿矾水解生成氢氧化亚铁不稳定,极易被氧化生成氢氧化铁;
D.氢氧化铁胶体具有吸附性,能够净水.
解答 解:A.氯气与水反应生成次氯酸,次氯酸具有杀菌消毒作用,所以可以用适量氯气杀菌消毒,故A正确;
B.绿矾中二价铁离子具有还原性,氯气能够氧化二价铁离子生成三价铁,故B正确;
C.绿矾水解生成氢氧化亚铁不稳定,极易被氧化生成氢氧化铁,所以明绿不具有净水作用,故C错误;
D.绿矾的氧化产物为硫酸铁,硫酸铁中三价铁水解生成氢氧化铁胶体,具有吸附性,能够净水,故D正确;
故选:C.
点评 本题考查了元素化合物知识,熟悉氯气、二价铁离子、三价铁离子性质是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | NO3- | B. | SO42- | C. | Na+ | D. | H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | V1=V2=V3 | B. | V1>V3>V2 | C. | V2>V3>V1 | D. | V1>V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
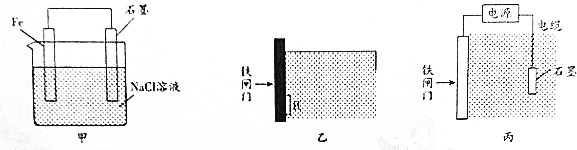
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
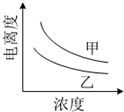 结合如表回答下列问题(均为25℃时的数据)
结合如表回答下列问题(均为25℃时的数据)| 酸 | 电力平衡常数(Ka) | 酸 | 电力平衡常数(Ka) |
| CH3COOH | 1.7×10-5 | H3BO3 | 5.8×10-10 |
| H2CO3 | Ka1=4.2×10-7 Ka2=5.6×10-11 | HNO2 | 7.1×10-4 |
| HCN | 6.2×10-10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com