
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见图,相关物质的沸点见附表)。其实验步骤为:
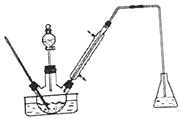
步骤1:将三颈瓶中的一定配比的无水AlCl3, 20mLl, 2 -二氯乙烷和20mL苯甲醛充分混合后.升温至60℃,缓慢滴加经H2SO4干燥过的液溴20mL,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,__________。
步骤3:有机相用10%NaHCO3溶液洗涤。经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。
(1)实验装置中冷凝管的主要作用是__________,锥形瓶中的溶液应为__________。
(2)步骤1所加入的物质中,AlCl3是催化剂,请推测1, 2-二氯乙烷的作用__________。
(3)有同学建议将装置中温度计换成搅拌器,那么温度计应移到什么地方__________。
(4)步骤2后续操作是__________。
(5)步骤3中用10%的NaHCO3溶液洗涤的具体操作是__________。加入无水MgSO4固体的作用是__________。
(6)步骤4中采用减压蒸馏技术,是为了防止__________。
(7)最后收集到间溴苯甲醛10mL,则该实验的产率为__________。
附表相关物质的沸点(101kPa)

【答案】(1)冷凝回流;NaOH;(2)溶剂;(3)水浴中;(4)搅拌、静置、分液;
(5)将有机相转移到分液漏斗中,向其中加入10%的NaHCO3溶液,充分振荡后分液,重复2-3次;除去有机相的水(6)间溴苯甲醛被氧化;(7)43.2%。
【解析】试题分析:(1)因溴易挥发,为使溴充分反应,应进行冷凝回流,以增大产率,反应发生取代反应,生成间溴苯甲醛的同时生成HBr,用氢氧化钠溶液吸收,防止污染空气,故答案为:冷凝回流;NaOH;
(2)将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合,三种物质中无水AlCl3为催化剂,1,2-二氯乙烷为溶剂,苯甲醛为反应物,故答案为:溶剂;
(3)有同学建议将装置中温度计换成搅拌器,那么温度计可以移到水浴中,控制温度,故答案为:水浴中;
(4)步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液,故答案为:搅拌、静置、分液;
(5)步骤3中用10%的NaHCO3溶液洗涤的具体操作为将有机相转移到分液漏斗中,向其中加入10%的NaHCO3溶液,充分振荡后分液,重复2-3次;经洗涤的有机相含有水,加入适量无水MgSO4固体,可起到除去有机相的水的作用,
故答案为:将有机相转移到分液漏斗中,向其中加入10%的NaHCO3溶液,充分振荡后分液,重复2-3次;除去有机相的水;
(6)减压蒸馏,可降低沸点,避免温度过高,导致间溴苯甲醛被氧化,故答案为:间溴苯甲醛被氧化;
(7)20mL苯甲醛的质量为21.2g,物质的量为![]() =0.2mol,20mL液溴的质量为60g,物质的量为
=0.2mol,20mL液溴的质量为60g,物质的量为![]() =0.375mol,分液后溴过量,苯甲醛完全反应生成0.2mol间溴苯甲醛,质量为0.2mol×185g/mol=37g,10mL间溴苯甲醛的质量为16g,产率为
=0.375mol,分液后溴过量,苯甲醛完全反应生成0.2mol间溴苯甲醛,质量为0.2mol×185g/mol=37g,10mL间溴苯甲醛的质量为16g,产率为![]() ×100%=43.2%,故答案为:43.2%。
×100%=43.2%,故答案为:43.2%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知咖啡酸的结构如图所示。关于咖啡酸的描述正确的是()

A.与该芳香族化合物分子式相同、官能团种类及数目均相同且苯环上的一氯代物只有两种的有机物的结构有4种(不考虑空间异构)
B.咖啡酸只能加聚成高分子化合物
C.咖啡酸最多可与5mol氢气发生加成反应
D.1mol该物质与足量的Na2CO3溶液反应,能消耗3 mol CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修2:化学与技术]
(1)我国某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
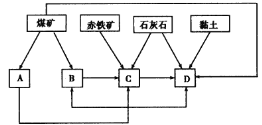
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定图中相应工厂的名称:A.________,B.________,C.________,D.________;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式:
__________________________________________________________;
。
(2)玻璃钢可由酚醛树脂和玻璃纤维制成。
①酚醛树脂由酚醛和甲醛缩聚而成,反应有大量热放出,为防止温度过高,应向有苯酚的反应釜________地加入甲醛,且反应釜应装有________装置。
②玻璃钢中玻璃纤维的作用是______。玻璃钢具有 等优异性能(写出两点即可)。
③下列处理废旧热固性酚醛塑料的做法合理的是________。
a.深埋 b.粉碎后用作树脂填料
c.用作燃料 d.用有机溶剂将其溶解,回收树脂
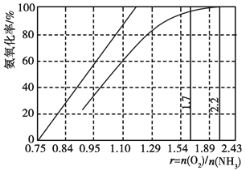
(3)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________,实际生产要将r值维持在1.7~2.2之间,原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。其正极反应方程式为________________。

(2)以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2molL﹣1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为 ;每消耗3.4g NH3转移的电子数目为_________。
(3)用NH3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的H2和I2(g)加入密闭容器中进行反应:H2+I2(g)![]() 2HI,反应进行到2min时测得反应速率υ(HI)=0.1mol/(L·min),I2(g)的物质的量浓度为0.4mol/L。
2HI,反应进行到2min时测得反应速率υ(HI)=0.1mol/(L·min),I2(g)的物质的量浓度为0.4mol/L。
(1)反应速率υ(I2)= 。
(2)2min未c(HI)= mol/L。
(3)起始时,c(H2)= mol/L,反应进行到2min时,容器中I2所占的体积分数是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月,屠哟哟获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。她成为首获科学类诺贝尔奖的中国人。青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯。下列有关说法正确的是

A.青蒿素分子式为C15H24O5
B.反应②原子利用率为100%
C.该过程中青蒿素生成双氢青蒿素属于氧化反应
D.1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5mol/L,可认为该离子不存在)。下列说法不正确的是

A.某温度下,CO2饱和溶液的浓度是0.05 molL-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度为0.1% ,
B.25℃时,H2CO3一级电离平衡常数的数值Ka1=10-6
C.向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)
D.25℃时,0.1mol/LNa2CO3中c(HCO3﹣)比0.1mol/LH2CO3中c(HCO3﹣)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用电镀污泥 (主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
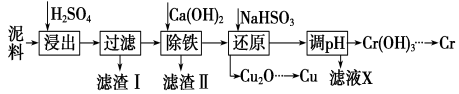
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
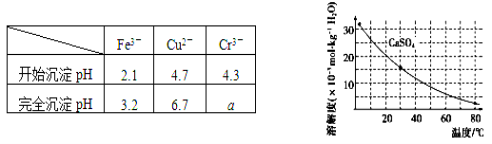
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有__________________。
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH到约________,检验Fe3+已经除尽的操作是_________________;
②将浊液加热到80℃,______________________。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式: ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是_______。
(4)当离子浓度小于或等于1×10-5mol·L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持 c(OH-)≥______。[已知:Ksp[Cr(OH)3]=6.3×10-31,![]() ≈4.0]。
≈4.0]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修2:化学与技术] 工业上可用食盐和石灰石为主要原料,经不同的方法生产纯碱。请回答下列问题:
(1)卢布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取,结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为: ;
②硫酸钠和焦炭、石灰石反应的化学方程式为: (已知硫酸钠做氧化剂,生成物中气体只有一种)。
(2)氨碱法的工艺如图所示,得到的碳酸氢钠经煅烧生成纯碱。

①图中的中间产物C是_______,(填化学式,下同)D是_______;
②装置乙中发生反应的化学方程式为 。
(3)联合制碱法是对氨碱法的改进,其优点是除了副产物氯化铵可用作化肥外还有______________。
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com