
【题目】(1)已知某盐酸溶液的密度为1.19g/cm3 ,质量分数为36.5%,则该溶液的物质的量浓度为___________
(2)含0.3 mol SO42-的Al2(SO4)3中所含的Al3+的数目为________________。
(3)相同质量的SO2、SO3硫原子的个数之比为_______________ 。
(4)33.3g某二价金属氯化物(ACl2)中含有0.6mol Cl,则ACl2的化学式是_________ 。
(5)标准状况下,1.204×1023个H2的体积约为_______________L
【答案】11.9mol/L 0.2NA 或 1.204×1023 5:4 CaCl2 4.48L
【解析】
(1)利用c=![]() =11.9mol·L-1;
=11.9mol·L-1;
答案为11.9mol·L-1;
(2)1molAl2(SO4)3中含有3molSO42-,因此含0.3molSO42-的Al2(SO4)3的物质的量为0.1mol,即n(Al3+)=0.1mol×2=0.2mol,含Al3+个数为0.2NA 或 1.204×1023;
答案为0.2NA 或 1.204×1023;
(3)根据SO2、SO3的化学式,SO2、SO3的物质的量与硫原子物质的量相等,令质量为xg,SO2的物质的量为![]() ,SO3的物质的量为
,SO3的物质的量为![]() ,硫原子物质的量之比等于硫原子个数比值,即硫原子个数比为
,硫原子物质的量之比等于硫原子个数比值,即硫原子个数比为![]() :
:![]() =5:4;
=5:4;
答案为5:4;
(4)1molACl2中含有2molCl-,则有:![]() =0.6mol,M=111g·mol-1,则A的摩尔质量为(111-35.5×2)g·mol-1=40g·mol-1,即A为Ca,化学式为CaCl2;
=0.6mol,M=111g·mol-1,则A的摩尔质量为(111-35.5×2)g·mol-1=40g·mol-1,即A为Ca,化学式为CaCl2;
答案为CaCl2;
(5)根据n=![]() ,氢气的物质的量为
,氢气的物质的量为![]() mol=0.2mol,则标准状况下的氢气的体积为0.2mol×22.4L·mol-1=4.48L;
mol=0.2mol,则标准状况下的氢气的体积为0.2mol×22.4L·mol-1=4.48L;
答案为4.48L。


科目:高中化学 来源: 题型:
【题目】聚乙烯醇肉桂酸酯(M)可用作光刻工艺中的抗腐蚀涂层,其合成路线如下:
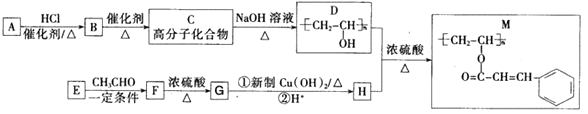
已知:

请回答:
(1)B的化学名称为_______________;M中含氧官能团的名称为_______________;F→G的反应类型为____________________。
(2)C→D的化学反应方程式为_________________________________________。
(3)E的结构简式为_______________;H的顺式结构简式为___________________。
(4)同时满足下列条件的F的同分异构体有_________种(不考虑立体异构):①属于芳香族化合物;②能发生水解反应和银镜反应。写出其中一种核磁共振氢谱有4种吸收峰,其峰面积之比为6:2:1:1的物质的结构简式_________。
(5)参照上述合成路线和相关信息,以乙烯和乙醛为原料(无机试剂任选)合成有机物![]() , 设计合成路线_____________。
, 设计合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中很多重要的原料都是来源于石油化工,回答下列问题

(1)C的结构简式为________。
(2)丙烯酸中含氧官能团的名称为_____________。
(3)③④反应的反应类型分别为_____________、___________。
(4)写出下列反应方程式
①反应①的化学方程式____________;
②反应②的化学方程式_________________;
③反应⑤的化学方程式____________。
(5)丙烯酸(CH2 = CH — COOH)可能发生的反应有_______________(填序号)
A 加成反应 B 取代反应 C 加聚反应 D 中和反应 E 氧化反应
(6)丙烯分子中最多有______个原子共面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是
A. 工业制硫酸采用二氧化硫催化氧化,高温可以提高单位时间SO3的产量
B. 合成氨工业中使用铁触媒做催化剂
C. 用饱和食盐水除去氯气中氯化氢杂质
D. 容器中有2NO2![]() N2O4,增大压强颜色变深
N2O4,增大压强颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有H2与O2的混合气体共0.6mol,该混合气体相对H2的密度为11,则下列说法正确的是( )
A.该混合气体的平均摩尔质量为11g/mol
B.混合气体中H2的物质的量为0.3mol
C.混合气体中O2的质量为12.8g
D.混合气体中H2和 O2的体积之比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼对植物的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
(1)区分晶体硼和无定硼形科学的方法为_________________________________。
(2)下列B原子基态的价层电子排布图中正确的是___________
A. B.
B.
C. D.
D.
(3)NaBH4是重要的储氢载体,阴离子的立体构型为___________。
(4)三硫化四磷分子(结构如下图1所示)是___________分子(填极性”或非极性)。
(5)图2表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为___________。

(6)硼酸晶体是片层结构,其中一层的结构如图3所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是_________________________________。
(7)立方氮化硼(BN)是新型高强度耐磨材料,可作为金属表面的保护层,其晶胞结构(如右图)与金刚石类似。已知该晶体密度为ag/cm3,则晶体中两个N原子间的最小距离为___________pm。(用含a的代数式表示,NA表示阿伏加德罗常数)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关环境问题的说法正确的是
A. 燃煤时加入适量石灰石,可减少废气中SO2的量
B. 臭氧的体积分数超过10-4%的空气有利于人体健康
C. pH在5.6—7.0之间的降水通常称为酸雨
D. 含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.10mol·L-1的H2C2O4(二元弱酸)溶液中滴加NaOH溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法不正确的是

A. 25℃时H2C2O4的一级电离常数为Ka1=104.3
B. pH=2.7的溶液中:c(H2C2O4)=c(C2O42-)
C. pH=7的溶液中:c(Na+)>2c(C2O42-)
D. 滴加NaOH溶液的过程中始终存在:c(OH-)+2c(C2O42-)+c(HC2O4-)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物污染是目前科学家们研究的热点问题之一。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___________;用尿素溶液也可吸收氮氧化物,研究表明,氮氧化物气体中NO的体积分数越大,总氮被还原率越低,可能的原因是______。
②在一个体积固定的真空密闭容器中充入等物质的量的CO2和NH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:
CO(NH2)2(s)+H2O(g)并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示:

则A点的v正(CO2)___________(填“>”“<”或“=”)B点的v逆(H2O),原因是________________。
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:2NO(g)+O2(g)=2NO2(g)△H1=akJ·mol-1,NO(g)+O3(g)=NO2(g)+O2(g)△H2=bkJ·mol-1,6NO2(g)+O3(g)===3N2 O5(g)△H3=c kJ·mol-1,则反应4NO2(g)+O2(g)=2N2O5(g)的△H=___________kJ·mol-1。
(3)氮氧化物也可用碱溶液吸收。若NO和NO2混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为_______;已知常温下,Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq)![]() NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
NaNO2(ag)+H2O(1)的平衡常数K=___________,相同物质的量浓度的HNO2、NaNO2混合溶液中,各离子的物质的量浓度由大到小的顺序为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com