
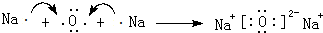 .
.分析 B离子和C离子有相同的电子层结构,二者可以形成C2B,说明B是第二周期元素,C是第三周期元素,所以B是O,C是Na;由于A离子比B离子多一个电子层,且可以形成AB2、AB3,所以A是S元素.
(5)H2、O2和NaOH溶液形成氢氧燃料电池,负极发生氧化反应,氢气再负极失去电子,碱性条件下生成水,本质是氢气燃烧生成水,根据H元素化合价变化计算转移电子,该电池在放电过程中,正极是氧气获得电子,碱性条件下生成氢氧根离子,原电池中电解质溶液里的阴离子向负极移动,阳离子向正极•
解答 解:B离子和C离子有相同的电子层结构,二者可以形成C2B,说明B是第二周期元素,C是第三周期元素,所以B是O,C是Na;由于A离子比B离子多一个电子层,且可以形成AB2、AB3,所以A是S元素.
(1)由上述分析可知,A为硫元素,故答案为:硫;
(2)用电子式表示Na2O的形成过程为: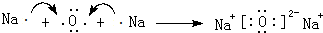 ,
,
故答案为: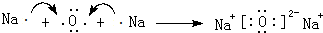 ;
;
(3)SO3熔点是16.8℃,沸点是44.8℃,标况下为固态,SO3的水化物为硫酸,在低温下跟Na2O2反应生成一种稳定性较差的过氧化物,该过氧化物为过氧化物,该反应的化学方程式是H2SO4+Na2O2=Na2SO4+H2O2,
故答案为:固;H2SO4+Na2O2=Na2SO4+H2O2;
(4)SO3的水化物溶液为硫酸,跟Na2S溶液反应的离子方程式是:2H++S2-=H2S↑,此反应物之一跟SO2反应的化学方程式是:2H2S+SO2=3S↓+2H2O,
故答案为:2H++S2-=H2S↑;2H2S+SO2=3S↓+2H2O;
(5)Na2O的水溶液为NaOH溶液,H2、O2和NaOH溶液形成氢氧燃料电池,负极发生氧化反应,氢气再负极失去电子,碱性条件下生成水,负极的电极反应为:2H2+4OH--4e-═4H2O,电极反应产生的水经冷凝后可作为航天员的饮用水,得到1.8L饮用水的物质的量为$\frac{1.8L×1000g/L}{18g/L}$=100mol,转移电子为200mol,则电池内转移的电子数为200 NA,该电池在放电过程中,正极是氧气获得电子,碱性条件下生成氢氧根离子,正极附近电解质溶液的pH将增大,电解质溶液里的OH-离子的移动方向是向负极移动,
故答案为:2H2+4OH--4e-═4H2O;200 NA;增大;负.
点评 本题考查元素周期表的结构以及元素周期律的应用,是高考中的常见题型,属于中等难度,解题的关键是掌握第1~18号元素名称和符号,元素同期表的结构,能根据元素同期律进行分析推断,有利于考查学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案科目:高中化学 来源: 题型:解答题
| 试管编号 | 3% Na2S2O3溶液 | H2O | 稀H2SO4(体积比为1:5) | 出现浑浊时间 |
| ① | 3mL | 3mL | 5滴 | 33s |
| ② | 4mL | 2mL | 5滴 | 28s |
| ③ | 5mL | 1mL | 5滴 | cs |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
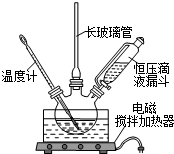 硝基苯是医药和染料的中间体,还可做有机溶剂.反应如下:
硝基苯是医药和染料的中间体,还可做有机溶剂.反应如下:
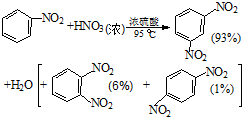
| 物质 | 熔点/ ℃ | 沸点 /℃ | 密度(20℃) /g•cm-3 | 水溶性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶 |
| 1,3二硝基苯 | 89 | 301 | 1.57 | 微溶 |
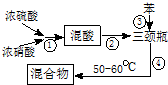

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
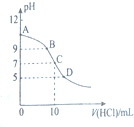 25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )
25℃时,NH3•H2O的电离平衡常数Kb=1.75×10-5,该温度下,用0.01mol•L-1盐酸滴定10mLamol•L-1氨水,盐酸的体积V(HCl)与溶液的pH关系如图所示,下列说法正确的是( )| A. | A点溶液中加少量水,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$减小 | |
| B. | 原氨水的物质的量浓度约为1.006×10-2mol•L-1 | |
| C. | B、D两点溶液中水电离出来的c(OH-):B<0 | |
| D. | C点溶液中的H2O不发生电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K层是能量最低的电子层 | |
| B. | 原子失电子时先失去能量低的电子 | |
| C. | 核外电子总是优先排布在能量较低的电子层上 | |
| D. | N层为次外层时,最多可容纳的电子数为18 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(O2)=0.001mol•L-1•s-1 | B. | v(NO)=0.0015 mol•L-1•s-1 | ||
| C. | v(H20)=0.003 mol•L-1•s-1 | D. | v(NH3)=0.001 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 配合物种类繁多,应用广泛.按要求完成下列各题:
配合物种类繁多,应用广泛.按要求完成下列各题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com