
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.2g D2中所含的电子的数目为2NA
B.标况下4.48L CHCl3中所含的原子数目为NA
C.4.4g CO2中所含的共用电子对数目为0.2NA
D.14 g 乙烯和环己烷(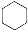 )的混合物中,所含碳原子数为NA
)的混合物中,所含碳原子数为NA
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源:2015-2016学年辽宁省大连市高二下期末化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.SO2和Cl2都能使品红溶液褪色,且加热后均恢复原色
B.SiO2是酸性氧化物,能与NaOH溶液反应
C.紫色石蕊试液滴入SO2水溶液中,先变红后褪色
D.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,则该溶液中一定含有SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省长沙市高二下期末理科化学试卷(解析版) 题型:选择题
常温下,下列各组离子能大量共存的是
A.pH=12的溶液中:K+、Na+、Br-、AlO
B.无色溶液中:MnO、H+、K+、C2O
C.c(Fe3+)=0.1 mol·L-1的溶液中:K+、H+、SCN-、I-
D.由水电离出的c(OH-)=1.0×10-13 mol·L-1的溶液中:Na+、NH、SO、HCO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省益阳市高一下期末化学试卷(解析版) 题型:选择题
为提纯下列物质(括号内为杂质),所用的除杂试剂和分离方法都正确的是( )
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
B | 苯(Br2) | NaOH溶液 | 过滤 |
C | C2H5OH(H2O) | 新制生石灰 | 蒸馏 |
D | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省益阳市高一下期末化学试卷(解析版) 题型:选择题
关于由锌片、铜片和稀硫酸组成的原电池的说法中,正确的是 ( )
A.电解质溶液的pH保持不变
B.电流方向是由锌片流向铜片
C.锌片作正极,发生还原反应
D.锌片质量逐渐减少,铜片上有气泡产生
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市河东区高一上期末化学试卷(解析版) 题型:实验题
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
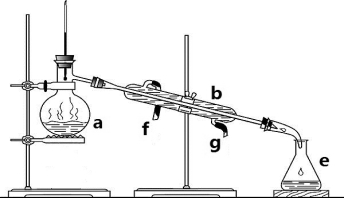
(1)写出下列仪器的名称:
a. b. e.
(2)仪器连接后,使用前必须进行的操作是 。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 ,将仪器补充完整后进行实验,温度计水银球的位置在 处。冷凝水由 (填f或g)口通入, 口流出。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市河东区高一上期末化学试卷(解析版) 题型:选择题
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤;正确的操作顺序是:
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高一下期末化学试卷(解析版) 题型:填空题
四种短周期元素A、B、C、D的性质或结构信息如下:
信息:①原子半径:A>B>C>D ②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲: 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二。
乙: 无色,无气味并且易燃。是常见的一种基础能源。
无色,无气味并且易燃。是常见的一种基础能源。
丙: 有强氧化性的弱酸,可以用于消毒杀菌。
有强氧化性的弱酸,可以用于消毒杀菌。
请根据上述信息回答下列问题。
(1)B元素在元素周期表中的位置为________________,请写出BC2分子的电子式:_______________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生反应:_____________________________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生反应:______________________________________________________。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入硫酸酸化的硫酸亚铁溶液。滴加过程中的现象为:
①试管中溶液变成深棕黄色,发生反应的离子方程式为 ;
②开始有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀。请回答“片刻后反应变得剧烈”的原因是a b
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:填空题
甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2=-58 kJ/mol
CH3OH(g)+H2O(g) △H2=-58 kJ/mol
③CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41 kJ/mol
CO(g)+H2O(g) △H3=+41 kJ/mol
回答下列问题:
(1)CO2的电子式是 。
(2)△H1= kJ/mol,①反应正向的熵变△S 0(填>、<或=)。
(3)在容积为2L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图像如图,下列说法正确的是__________(填序号)
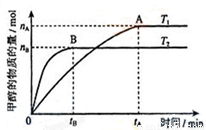
①温度为T1时,从反应到平衡,生成甲醇的平均速率为:v(CH3OH)=nA/tA mol/(L·min)
②当v(CH3OH) = v(H2O)时,说明反应达到平衡
③混合气体的平均相对分子质量A点大于B点
④处于A点的反应体系从T1变到T2,达到平衡时n(H2)与n(CH3OH)比值增大
(4)在T1温度时,将2molCO2和6molH2充入2L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,,则容器内的压强与起始压强之比为__________;T1温度,反应CH3OH(g)+H2O(g)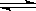 CO2(g)+3H2(g)的平衡常数数值为__________。
CO2(g)+3H2(g)的平衡常数数值为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com