
| A. | 乙烯和丙烷 | B. | 甲烷和丙烷 | C. | 甲烷和丙烯 | D. | 乙烯和丁烷 |
分析 将1.0体积混合气在氧气中充分燃烧,产生2.4体积CO2和2.8体积水蒸气,可知1mol混合气体含有2.4molC原子,5.6molH原子,则平均分子式是C2.4H5.6,利用C原子平均为2.4计算H原子平均数是否符合5.6,若符合平均分子式正确,否则错误.
解答 解:在相同条件下,气体的体积之比等于物质的量之比,将1.0体积混合气在氧气中充分燃烧,产生2.4体积CO2和2.8体积水蒸气,可知1mol混合气体含有2molC原子,5.6molH原子,则平均分子式是C2.4H5.6,
A.乙烯和丙烷若平均C原子数为2.4个,可假设乙烯为amol丙烷为bmol,$\frac{2×a+3×b}{a+b}$=2.4可以推出a:b=3:2,利用比例可以再求算出H原子平均数=$\frac{4×a+8×b}{a+b}$=$\frac{4×3+8×2}{3+2}$=5.6,平均分子式C2.4H5.6,故A正确;
B.甲烷和丙烷若平均C原子数为2.4个,同理可推出甲烷和丙烷的比例为3:7,可以推出H的个数为6.8,平均分子式为C2.4H6.8,故B错误;
C.甲烷和丙烯若平均C原子个数为2.4,同理可推出甲烷和丙烯的比例为3:7,可以推出H的个数为5.4,平均分子式为C2.4H5.4,故C错误;
D.乙烯和丁烷若平均C原子数为2.4个,同理可以推出乙烯和丁烷的比例为4:1,可推出H的个数为5.2,平均分子式为C2.4H5.2,故D错误;故选A.
点评 本题考查有机物的计算,侧重于学生的分析能力和计算能力的考查,难度不大,注意根据有机物的组成特点结合二氧化碳和水的体积关系计算有机物的平均分子式.


科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4NA | |
| B. | 将2mL 0.5mol/L Na2SiO3溶液滴入稀盐酸中制得H2SiO3胶体,所含胶粒数为0.001NA | |
| C. | 常温常压下,32gO2和O3的混合气体中含有的氧原子数为2NA | |
| D. | 25℃时,PH=13的Ba(OH)2溶液中含有OH-的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
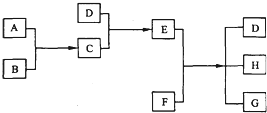
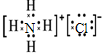
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com