
【题目】(1)4g氢气完全燃烧生成液态水时可放出572KJ的热量,氢气的燃烧热化学方程式: ___________。
(2)下图中该反应过程ΔH_____________0(填<或=或>);

(3)下图装置是由___________能转化为_____________能,负极电极反应式为:__________________,正极电极反应式为:_________________________________。

(4)如图用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为____________,若a电极产生56 mL气体(标况),则溶液中c(H+)=_____________(忽略溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入__________________(填字母)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3

【答案】H2(g)+1/2O2(g)=H2O(l) △H=-286kJ·mol-1 < 化学能 电能 H2-2e-+2OH-=2H2O O2+4e-+2H2O=4OH- 4OH--4e-=2H2O+O2↑ 0.1mol·L-1 AC
【解析】
(1)根据燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;根据n=m/M,计算1mol氢气完全燃烧放出的热量,结合热化学方程式的书写方法写出热化学方程式即可;
(2)生成物能量低,故反应放热,△H小于0;
(3)图中没有外接电源,是氢氧燃料电池;
(4)图是电解池,与电源正极连接的a电极为阳极,发生4OH--4e-═O2↑+2H2O,b为阴极,发生为Cu2++2e-═Cu,结合电极方程式计算.
(1)4g氢气的物质的量为:n=m/M=4g/2g·mol-1=2mol,2molH2在O2中完全燃烧生成2.00mol液态H2O放出572kJ的热量,所以1mol氢气完全燃烧放出热量286KJ,氢气燃烧热的热化学方程式为:H2(g)+1/2O2(g)=H2O(l) △H=-286kJ·mol-1;
(2)生成物能量低,故反应放热,△H小于0;
(3)图中没有外接电源,是原电池,图中装置是由化学转化为电能,负极还原剂失电子,电极反应式为:H2-2e-+2OH-=2H2O,正极是氧化剂得电子,电极反应式为:O2+4e-+2H2O=4OH-;
(4)图示电解100mL0.5mol·L-1CuSO4溶液,发生的电解池反应为:2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,与电源正极相连的为阳极,溶液中氢氧根离子失去电子发生氧化反应,电极反应为:4OH--4e-═2H2O+O2↑;
2Cu+O2↑+2H2SO4,与电源正极相连的为阳极,溶液中氢氧根离子失去电子发生氧化反应,电极反应为:4OH--4e-═2H2O+O2↑;
若a电极产生56mL(标准状况)气体为氧气,物质的量为0.0025mol,消耗氢氧根离子物质的量为0.01mol,溶液中生成氢离子物质的量为0.01mol,c(H+)=0.01mol/0.1L=0.1mol·L-1;
则所得溶液电解过程中CuSO4溶液每损失2个Cu原子,就损失2个 O原子,相当于损失一个CuO,为了使CuSO4溶液,恢复原浓度,应加入CuO,也可以加入CuCO3,符合恢复溶液浓度的定量关系,但不能加入Cu(OH)2、Cu2(OH)2CO3,因为CuCO3+H2SO4═CuSO4+CO2↑+H2O,相当于加CuO,而Cu(OH)2+H2SO4═CuSO4+2H2O、Cu2(OH)2CO3+2H2SO4═2CuSO4 +CO2↑+3H2O,除增加溶质外还增加了水;故选AC。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素X和Y形成能够离子化合物XY2。且该离子化合物中阴、阳离子具有相同的电子层结构。下列说法不正确的是( )
A.离子半径:X2+<Y-
B.原子序数:X<Y
C.该化合物中只存在离子键
D.原子最外层电子数X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个容积相同的恒容密闭容器中按不同的方式投入反应物,发生反应 N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ/mol,测得反应的相关数据如下表:
2NH3(g) △H=-92.4kJ/mol,测得反应的相关数据如下表:
容器甲 | 容器乙 | 容器丙 | |
反应温度/℃ | 400 | 400 | 500 |
反应物投入量 | 1molN2,3molH2 | 4molNH3 | 1molN2,3molH2 |
平衡时v(正)(H2)/mol/(Ls) | v1 | v2 | v3 |
平衡时c(NH3)/(mol/L) | c1 | c2 | c3 |
平衡时总压强P/Pa | P1 | P2 | P3 |
物质的平衡转化率a | a1(N2) | a2(NH3) | a3(N2) |
平衡常数K | K1 | K2 | K3 |
下列关系正确的是
A. v1<v2,c1<2c2 B. c2>2c3,a2(NH3)+a3(N2)<1
C. K1>K3, P2>2P3 D. v1<v3,a1(N2)<a3(N2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史。
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液)。
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙)。将“灰”溶于水可制得沤浸树皮脱胶的碱液。
③元代《庚道集》中记载:“点铜戍银”(即单质铜与砷融合形成银白色的物质)
请运用你学过的化学知识回答下列问题;
(1)在①~③中,发生了化学变化的是___(填编号)其中发生分解反应的化学方程式为___。
(2)①中发生变化的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒及其化合物在生产、生活中有着广泛的应用,掺杂硒的纳米氧化亚铜常用作光敏材料、电解锰行业催化剂等。
(1)酸性溶液中Na2SO3将H2SeO3和H2SeO4还原为晒单质的反应如下:
H2SeO3(aq)+2SO2(g)+H2O(l)=Se(s)+2H2SO4(aq) △H1
2H2SeO4(aq)+Se(s)+H2O(l)=3H2SO4(aq) △H2
H2SeO4(aq)+2SO2(g)+2H2O(l)=Se(s)+3H2SO4(aq) △H3
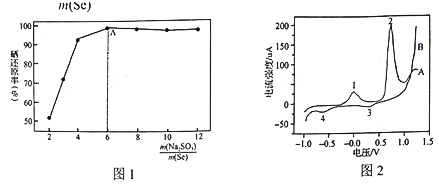
实验中控制其他条件不变(盐酸浓度等),![]() 与硒还原率关系如图1。在A点之前,随着
与硒还原率关系如图1。在A点之前,随着![]() 的增加,Se的还原率不断升高的原因是_____________。
的增加,Se的还原率不断升高的原因是_____________。
(2)向Na2SeO3溶液中加入适量的AgNO3溶液,得到Ag2Se纳米晶体,同时产生N2。该反应的离子方程式为 ______。
(3)制 PbSe 纳米管时还产生了副产物PbSeO3。己知:Ksp(PbSeO3)=3×l0-12, Ksp(PbSe)= 3×l0-38。为了除去PbSe中混有的PbSeO3,可以采取的措施是______。
(4)实验室测得碱性条件下PbSe纳米管在电极表面的氧化还原行为,结果如图2所示。其中一条曲线上的峰表示氧化过程,另一条曲线上的峰表示还原过程。整个过程共发生如下变化:Pb(OH)2—PbO2;Pb(OH)2—Pb; PbSe—Se; PbO2→Pb(OH)2,各物质均难溶于水。峰1对应的电极反应式为:PbSe-2e-+2OH-=Pb(OH)2+Se;则峰2对应的电极反应式为 ______。
(5)掺杂硒的纳米Cu2O催化剂可用于工业上合成甲醇:CO(g)+2H2(g)![]() CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
CH3OH(g) △H=akJ/mol。按n(H2):n(CO)=1:1的投料比将H2与CO充入VL的恒容密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的关系如下图所示。
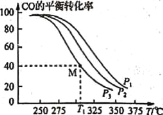
①压强P1、P2、P3由小到大的顺序是 __________。
②T1 ℃时若向该容器中充入2.0 mol H2和2.0 mol CO发生上述反应,5 min后反应达到平衡(M点),则M点对应条件下反应的平衡常数为 ______。
(6)将CuCl水解再热分解可得到纳米Cu2O。CuCl 水解的反应为 CuCl(s) +H2O(1) ![]() CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
CuOH(s)+Cl-(aq)+H+(aq),该反应的平衡常数 K与此温度下Kw、Ksp(CuOH)、Ksp(CuCl)的关系为K=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)![]() Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
Y(g)+Z(s),下列选项不能作为反应达到平衡标志的是
A. 反应容器中压强不再变化 B. 混合气体的密度不再变化
C. 混合气体的平均相对分子质量不再变化 D. Z的浓度不再改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)D在元素周期表中的位置是 。
(2)C2B的电子式是 ;AB2的结构式是 。
(3)B、C、E的离子半径由大到小的顺序为 (用化学式回答,下同);A、D、E元素最高价氧化物对应水化物的酸性由强到弱为 。
(4)B的气态氢化物与H2S相比沸点高的是 (用化学式回答);原因是 。
(5)水中锰含量超标,容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50gEB2时,共转移了1mol电子,则反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室中常见的气体制备、干燥和性质实验的部分仪器。

请回答下列问题:
(1)若实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳。
①所选仪器的连接顺序为______________________________(填写仪器序号字母)。
②生成二氧化碳的化学方程式为:____________________________。
(2)现有一混合气体,其主要成分为CO,含有少量水蒸气,还可能含有少量HCl气体。某化学课题组的同学欲用该混合气体进行实验:①检验HCl气体是否存在,并除去HCl气体②用干燥纯净的CO气体还原不纯的氧化铜试样(其中的杂质不发生变化)③检验CO气体还原氧化铜生成的气体生成物的性质。试用如图所示的仪器组装一套实验装置,完成上述实验任务。
①实验进行时,若要气体从左向右流动,则这几种仪器组件的连接顺序应是(填写仪器装置):_________。
②判定HCl气体是否存在的根据是___________________。
③若反应进行完全后,若仪器E中物质增重a g,则仪器D中的试样质量减少____g。
④若原混合气体中混有二氧化碳,反应进行完全后,若通过仪器E中物质增重来计算样品中氧化铜的纯度,测算结果将____(填“偏小”“偏大”“不受影响”之一)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各种变化是因为构成原电池的是( )
A.在空气中金属铝表面迅速氧化形成保护层
B.金属表面涂漆以阻止金属被氧化
C.红热的铁丝与水接触铁表面形成黑色物质
D.铁与稀硫酸反应时,加人少量硫酸铜溶液后可使反应速率加快
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com