
【题目】下列有关说法正确的是
A.CaCO3(s) =CaO(s)+CO2(g) 在室温下不能自发进行,说明该反应![]() H<0
H<0
B.水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应
C.0.1mol·L-1Na2CO3溶液在50℃时的碱性比25℃强,说明盐类水解反应是放热反应
D.蒸发FeCl3溶液,所得固体在坩埚中充分加热,最后得到Fe2O3固体
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为,![]() ,放电工作示意图如图。下列叙述不正确的是
,放电工作示意图如图。下列叙述不正确的是

A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:![]()
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式正确的是
A. AlCl3溶液中加入过量氨水:Al3++4NH3·H2O=AlO2-+2H2O+4NH4+
B. 碳酸的电离方程式:H2CO3![]() 2H++CO32-
2H++CO32-
C. 甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
D. 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲制备并探究![]() 的某些性质。
的某些性质。
(1)下列实验方案适用于在实验室制取所需![]() 的是________。
的是________。
A.![]() 溶液与
溶液与![]()
![]() 固体与浓硫酸
固体与浓硫酸
C.固体硫在纯氧中燃烧 ![]() 高温煅烧硫铁矿
高温煅烧硫铁矿
(2)探究二氧化硫的漂白性
甲同学用如图所示装置![]() 气密性良好
气密性良好![]() 进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。
进行实验,观察到如下现象:Ⅰ中红色褪去,Ⅱ中无变化。
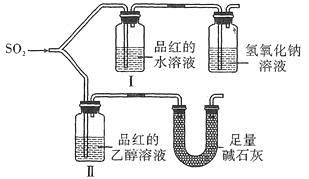
![]() 甲同学设计对照实验,但用足量碱石灰代替了氢氧化钠溶液,其原因是________________,根据实验现象得出的实验结论是_____________。
甲同学设计对照实验,但用足量碱石灰代替了氢氧化钠溶液,其原因是________________,根据实验现象得出的实验结论是_____________。
(3)乙同学设计用如图所示装置验证二氧化硫的化学性质。
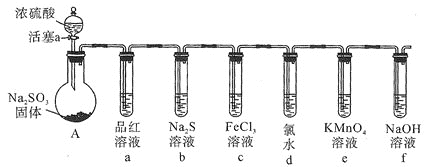
![]() 能说明二氧化硫具有氧化性的实验序号为________
能说明二氧化硫具有氧化性的实验序号为________![]() 填字母
填字母![]() 。
。
![]() 为了验证c中
为了验证c中![]() 与
与![]() 发生了氧化还原反应,在上图装置中通入过量的
发生了氧化还原反应,在上图装置中通入过量的![]() 后,取c中的溶液,分成三份,并设计了如下实验:
后,取c中的溶液,分成三份,并设计了如下实验:
方案Ⅰ:往第一份试液中加入酸性![]() 溶液,紫色褪去;
溶液,紫色褪去;
方案Ⅱ:往第二份试液中加入KSCN溶液不变红,再加入新制的氯水,溶液变红;
方案Ⅲ:往第三份试液中加入用盐酸酸化的![]() 溶液,产生白色沉淀。
溶液,产生白色沉淀。
指出上述不合理的方案并说明原因:______________________________________________。
![]() 试管e中发生反应的离子方程式为______________________________________________。
试管e中发生反应的离子方程式为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对分子性质的解释中,不正确的是( )
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 由于乳酸(![]() )中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
)中存在一个手性碳原子,导致该物质存在互为镜像的两个手性异构体
C. HF的稳定性很强,是因为其分子间能形成氢键
D. 由右图可知酸性:H3PO4>HClO,因为H3PO4分子中有1个非羟基氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究不同条件对相同体积相同物质的量浓度的 H2O2分解速率的影响,得到如下数据。由此不能得出的结论是:

A. Cu2+与 Fe3+对 H2O2 分解都有催化作用,但 Cu2+催化效果更好
B. 由Ⅰ与Ⅱ可知其它条件相同时,时间越长, H2O2 分解越彻底
C. 由Ⅰ与Ⅲ可知其它条件相同时,温度越高, H2O2 分解越快
D. 由Ⅰ与Ⅲ可知其它条件相同时,碱性越强, H2O2 分解越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某密闭容器内三种物质的浓度变化情况如图所示,其中P浓度的变化只表示出部分,若增大压强后N的百分含量不变,下列说法中正确的是
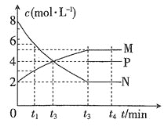
A.P可能是固体
B.![]() 时间段内平均反应速率υ(M)>υ(N)
时间段内平均反应速率υ(M)>υ(N)
C.![]() 时间段内,υ(P)=
时间段内,υ(P)=![]() mol·L-1·min-1
mol·L-1·min-1
D.该反应可表示为2N(g)M(g)+P(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近研制出可望成为高效火箭推进剂的![]() (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关![]() 的说法正确的是
的说法正确的是

A. 分子中N、O间形成的共价键是非极性键
B. 分子中四个氮原子共平面
C. 该物质既有氧化性又有还原性
D. 15.2g该物资含有6.02×![]() 个原子
个原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种重要的化工原料,已知A是一种卤代烃相对分子质量为92.5,其核磁共振氢谱中只有一个峰,C是一种高分子化合物,M是一种六元环状酯,转化关系如图所示,回答下列问题:
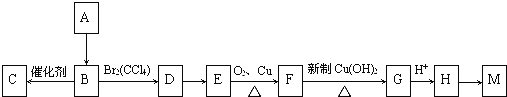
(1)A的分子式为 ;A→B的反应类型 ;
(2)有机物D的结构式为 . M的结构简式为 .
(3)写出下列反应的化学方程式:B→C: ;E→F: .
(4)写出满足下列条件的H的同分异构体d的结构简式 .
①属于酯类
②能发生银镜反应;
③能与金属钠反应放出气体;
④核磁共振氢谱有三个峰,且峰面积比为6:1:1.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com