
| A. | 三种意见都支持上述反应为氧化还原反应,且电子转移数相同 | |
| B. | 通过闻生成气体气味可判断反应快慢 | |
| C. | 用稀硫酸可鉴别硫代硫酸钠、亚硫酸钠溶液 | |
| D. | 生成的气体可漂白酸性高锰酸钾溶液 |
分析 A、(1)由于硫与亚硫酸钠加热可生成硫代硫酸钠,所以Na2S2O3中硫元素价态分别为0价,+4价,没有化合价发生变化;
B、根据Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O反应,可通过出现浑浊的时间长短判断反应快慢;
C、根据稀硫酸与硫代硫酸钠反应为Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O,与亚硫酸钠溶液Na2SO3+H2SO4=SO2↑+Na2SO4+H2O的现象分析判断;
D、二氧化硫具有强还原性与酸性高锰酸钾溶液具有强氧化性,两者发生氧化还原反应.
解答 解:A、(1)由于硫与亚硫酸钠加热可生成硫代硫酸钠,所以Na2S2O3中硫元素价态分别为0价,+4价,没有化合价发生变化,(2)(3)都有化合价变化支持上述反应为氧化还原反应,且电子转移数相同,故A错误;
B、根据Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O反应,可通过出现浑浊的时间长短判断反应快慢,不能通过闻生成气体气味判断,故B错误;
C、因为稀硫酸与硫代硫酸钠反应为Na2S2O3+H2SO4=S↓+SO2↑+Na2SO4+H2O会出现浑浊,而与亚硫酸钠溶液Na2SO3+H2SO4=SO2↑+Na2SO4+H2O无浑浊,据此可以鉴别,故C正确;
D、二氧化硫具有强还原性与酸性高锰酸钾溶液具有强氧化性,两者发生氧化还原反应而使酸性高锰酸钾溶液退色,不是漂白性,故D错误;
故选:C.
点评 本题考查了硫代硫酸钠的性质,难度不大,抓住反应前后化合价的变化及其产生的现象即可解题,注意氧化还原反应原理的应用.


科目:高中化学 来源: 题型:解答题
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
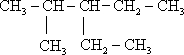 ;
;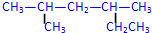 2,4-二甲基己烷
2,4-二甲基己烷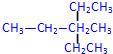 3-甲基-3-乙基戊烷
3-甲基-3-乙基戊烷 +2HNO3$→_{100-110℃}^{浓硫酸}$
+2HNO3$→_{100-110℃}^{浓硫酸}$ +2H2O.
+2H2O.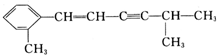 该分子中至少有8个C原子在同一平面,最多有13个C原子在同一平面.
该分子中至少有8个C原子在同一平面,最多有13个C原子在同一平面.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
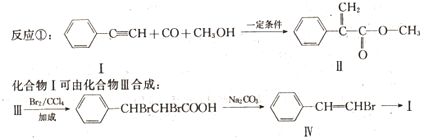
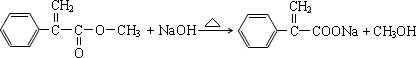 .
.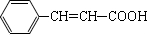 ,化合物Ⅳ通过消去反应生成化合物Ⅰ的化学方程式为
,化合物Ⅳ通过消去反应生成化合物Ⅰ的化学方程式为 .
.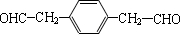 (写一种即可).
(写一种即可).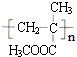 单体的结构简式为
单体的结构简式为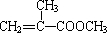 ;利用题中所给信息,自选合适的原料通过一步反应合成该单体,写出其化学方程式
;利用题中所给信息,自选合适的原料通过一步反应合成该单体,写出其化学方程式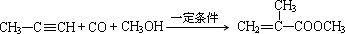 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
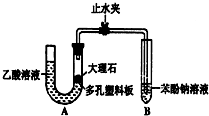 某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱并证明乙酸为弱酸,进行下述实验.
某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱并证明乙酸为弱酸,进行下述实验.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 $→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙
$→_{Ⅱ}^{一定条件}$Y$→_{Ⅲ}^{一定条件}$乙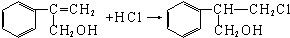 (不需注明反应条件).
(不需注明反应条件).
 .
. 、
、 、
、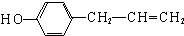 (其中一种).
(其中一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O═2HClO+CO32- | |
| B. | 向Fe(NO3)2和NaBr混合溶液中滴加稀盐酸:6Br-+8H++2NO3-═3Br2+2NO↑+4H2O | |
| C. | Na2S溶液中滴加NClO溶液:S2-+ClO-+H2O═S↓+Cl-+2OH- | |
| D. | 双氧水使酸性KMnO4溶液褪色:2MnO4-+5H2O2═2Mn2++5O2↑+6OH-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
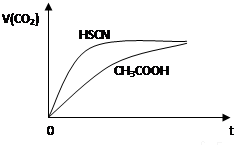
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com