
【化学——选修5:有机化学基础】
聚碳酸酯(D)可制作车、船、飞机的挡风玻璃。由A可合成聚碳酸酯(D)及食用香精(H)合成路线如下图所示(部分反应条件略去)。已知A、B中都只有一种化学环境的氢原子。请回答下列问题:
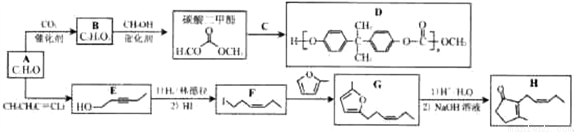
(1)A中的官能团名称为_____________。
(2)FG的反应类型为________________。
(3)1molH最多能与_____________molH2发生反应。
(4)C的结构简式为______________。
(5)由B生成碳酸二甲酯的化学方程式为___________。
(6)G的同分异构体中,符合以下条件的有____种:①能与FeCl3溶液发生显色反应;②苯环上只有2个取代基且互为对位。其中核磁共振氢谱只有5组峰的是_______(写结构简式)。
(7)请根据题中信息设计简要合成路线以CH3C=CLi、乙醇和上述路线图中的个别物质合成1,3-戊二烯。合成路线流程图示例如下:________
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:选择题
下列由于物质的漂白性而导致溶液褪色的是( )
①将过氧化钠投入水中,然后加入几滴酚酞溶液,溶液先变红后褪色
②将活性炭放入红墨水中,溶液褪色
③向品红溶液中滴加氯水,红色褪去
④向酸性高锰酸钾溶液中通入二氧化硫气体,溶液紫色褪去
A. ①③ B. ①②③ C. ①②③④ D. ②④
查看答案和解析>>
科目:高中化学 来源:2017届湖南省衡阳市高三实验班第六次月考理综化学试卷(解析版) 题型:选择题
在一定温度下,容积固定的密闭容器中,通入一定量的N2O4,发生反应N2O4(g)  2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
2NO2(g),体系中各物质浓度随时间变化如图所示,则下列叙述错误的是
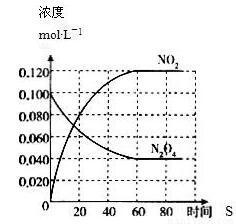
A. 若温度升高,混合气体的颜色变深
B. 在该温度下反应2NO2(g)  N2O4(g)的平衡常K为25/9
N2O4(g)的平衡常K为25/9
C. 反应达平衡后,将反应容器的容积减少一半,平衡向正反应方向移动
D. 反应达平衡后,向此容器中通入NO2气体,则c(NO2)增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:选择题
有aXn-和bYm+两种简单离子,且X、Y均为短周期元素,已知Xn-比Ym+多2个电子层,下列关系和说法正确的是( )
A. Y可能是第二周期元素 B. a-b+n+m的和只可能等于10
C. b大于 5 D. X只能是第三周期元素
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高一3月月考化学试卷(解析版) 题型:选择题
下列说法中不正确的是( )
①质子数相同的粒子一定属于同种元素;
②同位素的性质几乎完全相同;
③质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子;
④电子数相同的粒子不一定是同一种元素;
⑤一种元素只能有一种质量数;
⑥某种元素的相对原子质量取整数,就是其质量数
⑦元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
⑧核外电子排布相同的微粒化学性质不一定相同
⑨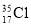 与
与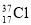 得电子能力相同
得电子能力相同
A. ①②④⑤ B. ③④⑤⑥ C. ②③⑤⑥ D. ①②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三3月月考理科综合化学试卷(解析版) 题型:选择题
利用下图装置收集气体并验证其某些化学性质,正确的是
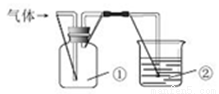
选项 | 气体 | 试剂② | 现象 | 结论 |
A | NH3 | 酚酞试液 | 溶液变红色 | NH3的水溶液显碱性 |
B | Cl2 | 紫色石蕊试液 | 溶液立即褪色 | Cl2有氧化性 |
C | SO2 | 溴水 | 溶液褪色 | SO2有漂白性 |
D | X(能形成酸雨) | KI淀粉溶液 | 溶液变蓝 | X是NO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:河北省2017届高三下学期三调考试理科综合化学试卷 题型:填空题
烯烃在化工生产过程中有重要意义。下面是以烯烃A为原料合成粘合剂M的路线图。

回答下列问题:
(1)下列关于路线图中的有机物或转化关系的说法正确的是_______(填字母)。
A. A能发生加成、氧化、缩聚等反应
B.B的结构简式为CH2ClCHClCH3
C. C的分子式为C4H5O3
D. M的单体是CH2=CHCOOCH3和CH2=CHCONH2
(2)A中所含官能团的名称是_______,反应①的反应类型为_________。
(3)设计步骤③⑤的目的是_________, C的名称为________。
(4)C和D生成粘合剂M的化学方程式为____________。
(5)满足下列条件的C的同分异构体共有__种(不含立体异构),写出其中核磁共振氢谱有3组峰的同分异构体的结构简式:_____________。
①能发生银镜反应 ② 酸、碱性条件下都能水解 ③ 不含环状结构
(6)结合信息,以CH3CH=CHCH2OH为原料(无机试剂任选),设计制备CH3CH=CHCOOH的合成路线。合成路线流程图示例如下:_____________
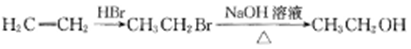
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省太原市高一3月阶段性测试化学试卷(解析版) 题型:选择题
将铜和镁组成的2.24g混合物投入适量某浓度的硝酸中完全反应,还原产物中有NO2、NO、N2O三种气体,且体积均为0.224L(标准状况),然后向反应后的溶液中,加入足量的NaOH溶液,所得沉淀经过滤、洗涤、干燥后称量,质量为
A. 3.12g B. 4.28g C. 4.68g D. 5.08g
查看答案和解析>>
科目:高中化学 来源:南开中学2016-2017高三第四次月考理综化学试卷 题型:填空题
平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题以此粉末为原料,设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵:
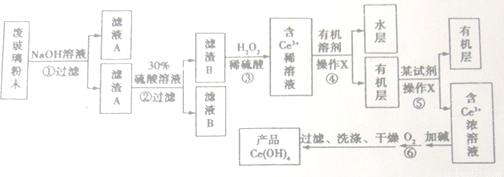
己知:
I.酸性条件下,铈在水溶液中有Ce3+、Ce4+两种主要存在形式;
II. CeO2不溶于稀硫酸;利用有机溶剂可分离稀土元素如Ce等化合物。
请按要求回答下列问题:
(1) Ce的原子序数为58,它位于元素周期表中第______周期。
(2)步骤①、⑥反应的化学方程式分别为_________________、______________。
(3)检验滤渣B洗涤干净的方法是____________________。
(4)步骤③的离子方程式为____________________。
(5)操作X名称为_________________。
(6)在滤液B中加过量铁粉于50 °C水浴中加热充分反应后趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口,静置、冷却一段时间后收集得产品绿矾。
步骤②中的硫酸溶液过稀会导致____________;静置冷却一段时间后,在试管中观察到的现象是______________________。
(7)取2.08 g产品Ce(OH)4加过量稀硫酸溶解后,用0.1000 mol/L FeSO4溶液滴定至终点共消耗90.00mL,则产品中Ce(OH)4的质量分数为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com