
(10分)氢是一种重要的非金属元素。氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)工业上一般采用CO和H2反应合成可再生能源甲醇。反应如下:
CO(g) + 2H2(g)  CH3OH(g) ΔH= -90.1KJ·mol-1
CH3OH(g) ΔH= -90.1KJ·mol-1
在250℃下,将一定量的CO和H2投入10L的密闭容器中,各物质的物质的量浓度(mol·L-1)变化如下表所示:(前6min没有改变条件)
2min | 4min | 6min | 8min | … | |
CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
H2 | x | 0.12 | 0.12 | 0.20 | … |
CH3OH | 0.03 | 0.04 | 0.04 | 0.05 | … |
①x= 。
②250℃时该反应的平衡常数K的计算式为: (不必化简)。
③若6min~8min只改变了某一条件,所改变的具体条件是 。
④第8min时,该反应是不是达到平衡状态 。(填“是”或“不是”)
(2)某硝酸厂处理尾气中的NO的方法是用H2将NO还原为N2。已知:

H2还原NO生成氮气和水蒸气的热化学方程式是 。
(10分,每空2分) (1)①x=0.14 ②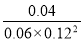 ③加1 mol氢气 ④ 不是
③加1 mol氢气 ④ 不是
(2)2NO(g)+2H2(g)=N2(g)+2H2O(g) ΔH=-665 kJ·mol-1
【解析】
试题分析:(1)①根据表中数据可知2min至4min时消耗CO是0.01mol/L×10L=0.1mol,则根据方程式可知同时消耗氢气是0.2mol,所以x=0.02+0.12=0.14。
②根据表中数据可知反应进行到4min时达到平衡状态,此时CO、氢气、甲醇的浓度分别是0.006mol/L、0.012mol/L、0.004mol/L,实验平衡常数K=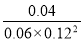 。
。
③6min时CO浓度减小,氢气和甲醇浓度增加,且CO浓度减小0.01mol/L,氢气浓度增加0.08mol/L,所以若6min~8min只改变了某一条件,所改变的具体条件是加1mol氢气。
④第8min时,CO、氢气和甲醇的浓度分别是0.05mol/L、0.20mol/L、0.05mol/L,则此时浓度商=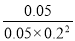 ≠
≠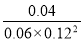 ,因此不是平衡状态。
,因此不是平衡状态。
(2)由于反应热等于断键吸收的能量与形成化学键说放出的能量的差值,所以根据关系图可知该反应的反应热=2×630 kJ·mol-1+2×436 kJ·mol-1—945 kJ·mol-1—4×436 kJ·mol-1=—665 kJ·mol-1,所以热化学方程式为2NO(g)+2H2(g)=N2(g)+2H2O(g) ΔH=-665 kJ·mol-1。
考点:考查可逆反应与反应热的有关计算


科目:高中化学 来源:2014-2015学年湖南省高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列离子反应方程式中,书写正确的是
A.过量明矾溶液加入偏铝酸钠溶液:Al3++3AlO2-+6H2O=4Al(OH)3↓
B.氯化铁溶液与适量铜粉混合:Cu + Fe3+ = Cu2++ Fe2+
C.Fe3O4固体溶于足量稀硝酸溶液中:Fe3O4+8H+=2Fe3++ Fe2++ 4H2O
D.碳酸氢铵溶液与足量澄清石灰水溶液混合:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省天一高三上学期大联考化学试卷(解析版) 题型:选择题
甲醇(CH3OH)是一种有毒物质,检测甲醇含量的测试仪工作原理示意图如下。下列说法正确的是

A.该装置为电能转化为化学能的装置
B.a电极发生的电极反应为CH3OH+H2O-6e-═CO2↑+6H+
C.当电路中有1 mol e-转移时,正极区n(H+)增加1 mol
D.将酸性电解质溶液改为碱性电解质溶液该测试仪不可能产生电流
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省天一高三上学期大联考化学试卷(解析版) 题型:选择题
近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、高锰酸钾溶液、次氯酸钠溶液、双氧水等消毒剂可以完全灭活病毒感染性。下列有关说法正确的是
A.乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
B.高锰酸钾溶液和双氧水的消毒原理相同
C.双氧水具有较强的腐蚀性,不能用于皮肤的消毒
D.在次氯酸钠溶液中通入少量二氧化硫可得到亚硫酸钠和次氯酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
下列图示与对应的叙述相符的是




A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.图丙表示催化剂能改变化学反应的焓变
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g) N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省邯郸市高三上学期1月教学质量检测化学试卷(解析版) 题型:选择题
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示。已知Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是

A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>W>X
C.氢化物的稳定性:X>Y>Z
D.四种元素的常见单质中,Z单质的熔、沸点最高
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省高三上学期期末理综化学试卷(解析版) 题型:选择题
下列各组离子,一定能在指定环境中大量共存的是
A.在含有大量I-离子的溶液中:Cl?、Fe3+、Al3+、Cu2+
B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存
C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl?、Br?
D.在加入Al能放出大量H2的溶液中:NH4+、SO42? 、C1?、HCO3?
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省名校新高考研究联盟高三上学期联考化学试卷(解析版) 题型:选择题
我国发射载人航天飞船用于火箭启动炸药的是氕化锂、氘化锂和氚化锂,它们
A.都是共价化合物
B.都具有较强还原性
C.由同位素原子构成的同分异构体
D.微粒的半径H-小于Li+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com