
����Ŀ��̼����(MnCO3) ������ĸ�����ǿ���Բ��ϣ�Ҳ���Ʊ�Mn2O3��MnO2���̵����������Ҫԭ�ϣ��㷺���ڵ��ӡ�������ҽҩ����ҵ��
(1) ��ҵ���Ʊ�����ʽΪ��MnSO4+2NH4HCO3=MnCO3 ��+ (NH4)2SO4+CO2 ��+H2O����Ӧ��ͨ��������Թ�����NH4HCO3���ҿ�����Һ��pHΪ6.8~7.4�������Թ�����NH4HCO3��Ŀ����_____��
(2) ʵ����ģ�ҵ���������Ʊ�������װ����ͼ4��ʾ��

��ʯ�����������________��
����Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ��________��
(3) MnCO3 �ڿ����м�����ת��Ϊ��ͬ��̬���̵���������������������¶ȵı仯��ͼ5 ��A��B��C��D ����ʾ����300��ʱ��ʣ���������Ԫ������Ԫ�ص����ʵ���֮�ȼ�n(Mn) :n(O)Ϊ_______�� ͼ�е�D ��Ӧ����ijɷ�Ϊ______ (�ѧʽ)��

���𰸡� ʹMnSO4��ַ�Ӧ�����MnSO4����������NH4HCO3�ֽ� ���ն����SO2�����ٶԻ�������Ⱦ ����ͨ����������� 1:2 Mn3O4��MnO
��������������������⿼�鷴Ӧ�����Ŀ��ƣ���SO2�йص�ʵ�飬����ͼ����ļ��㡣
��1�������Թ�����NH4HCO3����ʹMnSO4��ַ�Ӧ�����MnSO4�������ʣ�NH4HCO3�ֽ�������NH4HCO3Ҫ�Թ�����
��2��������װ��ͼ����������ƿ��SO2��MnO2��Ӧ�Ƶ�MnSO4������SO2��Ⱦ��������ʯ�������ն����SO2�����ٶԻ�������Ⱦ����ӦΪSO2+Ca��OH��2=CaSO3+H2O��
����Ӧ�����У�ΪʹSO2������ת����ȫ����ͨ��SO2��N2����һ�������ı��ҺͶ�ϵ������£��ɲ�ȡ�ĺ�����ʩ��������ͨ��������ʹ���������MnO2������ã��ʵ������¶���
��3����MnCO3���ʵ���Ϊ1mol��m��MnCO3��=1mol![]() 115g/mol=115g������n��Mn��=1mol��300����ʣ����������Ϊ115g
115g/mol=115g������n��Mn��=1mol��300����ʣ����������Ϊ115g![]() 75.65%=87g������m��O��=87g-55g=32g��n��O��=32g
75.65%=87g������m��O��=87g-55g=32g��n��O��=32g![]() 16g/mol=2mol��n��Mn����n��O��=1:2����ͼ�ɼ�D�������B���C��Ĺ����϶��ɣ�B�㣬ʣ����������Ϊ115g
16g/mol=2mol��n��Mn����n��O��=1:2����ͼ�ɼ�D�������B���C��Ĺ����϶��ɣ�B�㣬ʣ����������Ϊ115g![]() 66.38%=76.34g������n��O��=
66.38%=76.34g������n��O��=![]() =1.334mol��n��Mn����n��O��=1mol��1.334mol=3:4��B�����ΪMn3O4��C�㣬ʣ����������Ϊ115g
=1.334mol��n��Mn����n��O��=1mol��1.334mol=3:4��B�����ΪMn3O4��C�㣬ʣ����������Ϊ115g![]() 61.74%=71g������n��O��=
61.74%=71g������n��O��=![]() =1mol��n��Mn����n��O��=1mol��1mol=1:1��C�����ΪMnO��D���Ӧ����ɷ�ΪMn3O4��MnO��
=1mol��n��Mn����n��O��=1mol��1mol=1:1��C�����ΪMnO��D���Ӧ����ɷ�ΪMn3O4��MnO��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ��ʾ���з�Ӧ�����ӷ�Ӧ����ʽΪ�� ��
A��NH4HCO3����������ŨKOH��Һ�У�NH4++ HCO3-+2OH-= CO32-+ NH3��+2 H2O
B����������������ϡ���3Fe2����4H����NO3��![]() 3Fe3����NO����3H2O
3Fe3����NO����3H2O
C��FeBr2��Һ������ʵ�����Cl2��Ӧ��2Fe2����2Br����2Cl2===2Fe3����4Cl����Br2
D��H2SO4��Ba(OH)2��Һ��Ӧ��Ba2����OH����H����SO![]() ===BaSO4����H2O
===BaSO4����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ԫ��X��Y��Z��W��ԭ��������������Xԭ�Ӻ��������������Ǵ�����2����Y�ķ�����YF3�����и�ԭ�Ӿ��ﵽ8�����ȶ��ṹ��Z��ͬ������ԭ�Ӱ뾶����Ԫ�أ�W���������Ϊ+7�ۡ�����˵����ȷ����
A. �����Ӱ뾶��С˳��: rX>rZ>rY
B. Ԫ��W���������Ӧˮ��������Ա�Y��ǿ
C. X��Y�γɵ�ԭ�Ӿ���X3Y4���۵�Ƚ��ʯ��
D. X��W�γɵĻ������Z��W�γɵĻ�����Ļ�ѧ��������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������䡱�������������ص㹤�̣������������ָ��Ȼ��������Ҫ�ɷ��Ǽ��飮��ҵ�Ͻ�̼��ˮ�ڸ����·�Ӧ�Ƶ�ˮú����ˮú������Ҫ�ɷ���CO��H2 �� ���ߵ������ԼΪ1��1����֪1mol CO������ȫȼ������CO2����ų�283kJ������1molH2��ȫȼ������Һ̬ˮ�ų�286kJ������1molCH4 ������ȫȼ������CO2�����Һ̬ˮ�ų�890kJ������
��1��д��H2��ȫȼ������Һ̬ˮ���Ȼ�ѧ��Ӧ����ʽ�� �� ��1molCH4������ȫȼ������CO2�����ˮ�������ų������� 890kJ�����������=��������
��2������ˮú���������ɷ֣���ͬ״�������õ���ȵ�����������ˮú�������������ԼΪ��ȼ�����ɵ�CO2 ��������ԼΪ ��
��3���������ݺͼ���˵��������Ȼ������ˮú��������ȼ�ϣ�ͻ�����ŵ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʷ����������ȷ����( )
A.CaCl2��NaOH��HCl��O2�������ʶ����ڻ�����
B.���ᡢ��������ƺ���ʯ�ҷֱ������ᡢ��κ�������
C.��Һ����Һ�����嶼���ڻ����
D.CO2��CO�ȷǽ������������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1) ��֪: CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H1 = akJ/mol��
CO(g) + H2O (g)=CO2(g) + H2 (g) ��H2 = bkJ/mol��
2CO(g) + O2(g)= 2CO2(g) ��H3 = ckJ/mol��
��ӦCO2(g)+ CH4(g)=2CO(g) + 2H2(g) ����H = _____kJ/mol��
(2) ��ѧ���õ����ز�����ͭ��װ��ͼ10���˹����ϵͳ�����ø�װ�óɹ���ʵ������CO2��H2O�ϳ�CH4��
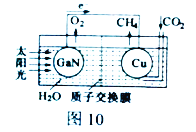
��д��ͭ�缫����ĵ缫��Ӧʽ_____________��
��Ϊ��߸��˹����ϵͳ�Ĺ���Ч�ʣ�����װ���м�������_______ (ѡ��������������������)��
(3) ��Ȼ���е�H2S ���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS ��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽ___________��
(4) ���������Ӧ�����Ʊ�CS2����������ͼ11��ʾ:
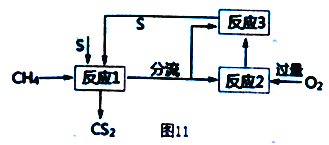
��д��������Ӧ1�Ļ�ѧ��Ӧ����ʽ___________��
����Ӧ1�������ֺ�������ʣ�Ϊ�����CS2�IJ��ʣ���Ʒ�Ӧ2��3ʵ������ѭ�����ã�ʵ��ʱ��Է�Ӧ1�������������������뷴Ӧ2 �ͷ�Ӧ3 ���������ʵ���֮��Ϊ___________��
������Ӧ1��ÿ��1molCS2����ʱ����Ӧ2����Ҫ����O2�����ʵ���Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������2030��ǻ�ʯ��Դռһ����Դ���ѱ��ؽ���ߵ�20%���ң����в����ڻ�ʯ��Դ���ǣ�������
A.ú
B.��������
C.��Ȼ��
D.ʯ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I�����Ǽ���ʵ���г��õ�������
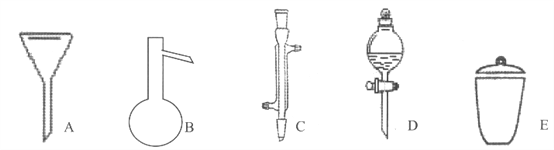
д����������������������ƣ�
A__________��B__________��C__________��D__________��E__________
IIʵ����Ҫ����100 mL 2 mol��L NaCl��Һ����ش��������⣺
��1�����ƹ�������Ҫʹ�õ���Ҫ�������������ձ�������������ͷ�ιܡ���ƽ����Ͳ��__________________��
��2����������ƽ��ȡ�Ȼ��ƹ��壬������Ϊ__________g��
��3��������Ҫ�����������ȷ˳����____________________������ţ���
�ٳ�ȡһ���������Ȼ��ƣ������ձ��У�����������ˮ�ܽ⣻
�ڼ�ˮ��Һ��������ƿ���̶�����1��2����ʱ�����ý�ͷ�ιܵμ�����ˮ����Һ����̶������У�
�۽���Һת�Ƶ�����ƿ�У�
�ܸǺ�ƿ�����������µߵ���ҡ�ȣ�
������������ˮϴ���ձ��ڱںͲ�����2��3�Σ�ϴ��Һת�Ƶ�����ƿ�С�
��4�����ʵ�������ȱ�ٲ���ݣ������������Һ�����ʵ���Ũ��__________ ���ƫ�ߡ���ƫ�͡�����Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ�����ڱ���һ����,����EΪ�ؿ��к�����ߵ�Ԫ�ء�
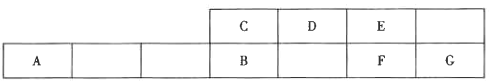
�������������:
��1��DԪ����Ԫ�����ڱ��е�λ��: _______��
��2��A��E�����ӵİ뾶�ɴ�С˳��Ϊ_______(�þ���������ű�ʾ,��ͬ) ��
��3��д��A��F����Ԫ�ص�����������ˮ�������Ӧ�����ӷ���ʽ_______��
��4����ҵ��C�ĵ����� B������������Ʊ�B���ʵĻ�ѧ����ʽ_______��
��5��֤��Ԫ��F��G�ķǽ�����ǿ��(�û�ѧ����ʽ��ʾ) _______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com