
| A、稳定性:W的氢化物>Z的氢化物,沸点:W的氢化物<Z的氢化物 |
| B、元素X、Y、Z的单质晶体可能属于同种类型的晶体 |
| C、XZ2、X2M2、M2Z2均为直线型的共价化合物 |
| D、由Z和W组成的一种化合物能使酸性高锰酸钾溶液褪色,表明其具有漂白性 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 选项 | 实验事实 | 结论 |
| A | 将二氧化硫通入溴水中,溴水褪色 | 二氧化硫有漂白性 |
| B | 淀粉与稀硫酸共热,再加银氨溶液水浴加热,无银镜生成 | 淀粉没有水解 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向1mL 0.1mol/L的AgNO3溶液中加入1mL 0.1mol/L NaCl溶液,出现白色沉淀,再加几滴0.1mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||||
B、
| ||||
| C、常温常压下,只有一种元素的单质是液态 | ||||
| D、常温常压下,气态单质的分子都是由非金属元素的原子形成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应能够制造新物质,同时也能制造出新的元素 |
| B、煤在空气中强热得到焦炭、煤焦油、焦炉气、粗氨水等产物的过程叫煤的干馏 |
| C、在酿酒的过程中,葡萄糖可通过水解反应生成酒精 |
| D、工业生产玻璃、水泥、冶炼铁均需要用到石灰石为原料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关该溶液的叙述不正确的是( )
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关该溶液的叙述不正确的是( )| A、pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B、溶液中:c(H+)+c(Na+)=c(CH3COO-)+c(OH-) |
| C、由W点可以求出25℃时CH3COOH的电离常数 |
| D、pH=4的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
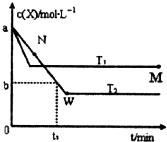 在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )| A、该反应进行到M点放出的热量大于进行到W点放出的热量 | ||
B、T2下,在0?t1时间内,υ(Y)=
| ||
| C、M点的平衡常数比W点的平衡常数小 | ||
| D、M点时再加入一定量的X,平衡后X的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验目的 | 仪器 |
| A | 从食盐水中获得NaCl晶体 | 蒸发皿、玻璃棒、酒精灯 |
| B | 用硫酸、Na2CO3溶液比较元素S与C的非金属性强弱 | 试管、胶头滴管 |
| C | 用8.0mol.L-1的盐酸配制250mL1.5mol.L-1的盐酸 | 250mL容量瓶、玻璃棒、烧杯 |
| D | 测定NaOH溶液的物质的量浓度 | 酸(碱)式滴定管、胶头滴管、锥形瓶、烧杯 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com