
| A. | 单质的沸点:A>B | B. | B与C不能存在于同一离子化合物中 | ||
| C. | 氧化物的水化物的酸性:C<D | D. | 阴离子的半径:C>D |
分析 A、B、C、D均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,则A是H元素,B是N元素,C、D处于第三周期,四元素原子的最外层电子数之和为19,C、D最外层电子数之和是19-1-5=13,最外层电子数只能为6、7,又C原子序数小于D,则C是S元素、D是Cl元素,据此解答.
解答 解:A、B、C、D均为的短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,则A是H元素,B是N元素,C、D处于第三周期,四元素原子的最外层电子数之和为19,C、D最外层电子数之和是19-1-5=13,最外层电子数只能为6、7,又C原子序数小于D,则C是S元素、D是Cl元素.
A.H、N元素单质都是分子晶体,分子晶体熔沸点与相对分子质量成正比,氮气相对分子质量大于氢气,所以单质的沸点:A<B,故A错误;
B.B是N元素,C是S元素,两种元素能存在于同一离子化合物中,如硫酸铵中,故B错误;
C.元素的非金属性越强,其最高价氧化物的水化物酸性越强,非金属性S<Cl,最高价氧化物的水化物酸性H2SO4<HClO4,但氧化物的水化物的酸性不一定存在此规律,如亚硫酸酸性大于次氯酸,故C错误;
D.核外电子排布相同的离子,原子序数越大,离子半径越小,则阴离子的半径:C>D,故D正确;
故选D.
点评 本题考查原子结构和元素性质,涉及离子化合物判断、酸性强弱判断、离子半径的比较、元素周期律等知识点,正确判断元素是解本题关键,易错选项是C,学生容易忽略最高价含氧酸.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:解答题
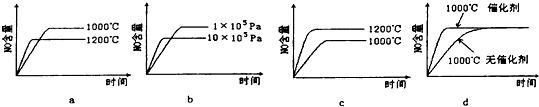
| 时间/浓度 | c(NH3)(mol/L) | C(O2)(mol/L) | C(NO)(mol/L) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.8 | 0.975 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,在恒容密闭容器中充入等体积的X、Y气体,发生反应X(g)+Y(g)?2Z(g),一段时间后达到平衡,其他条件不变,再充入0.3mol Z,平衡时Y的体积分数增大 | |
| B. | 碱性锌锰干电池工作过程中,每通过2mol电子,负极质量减轻130g | |
| C. | 通过测定CH3COONa溶液和NaHS溶液的pH,可以比较醋酸和氢硫酸酸性的强弱 | |
| D. | 将MgCl2、Mg(OH)2、MgCO3三种物质与水混合,加热、灼烧,最终的固体产物相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2属于危险化学品,其标识应为: | |
| B. | 当你走进化学实验室之前,应认真阅读实验室的安全守则 | |
| C. | 中国大陆的火警报警电话为“119”,香港、澳门为“999” | |
| D. | 一般情况下,金属类物质着火时不宜使用二氧化碳类灭火器 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na的密度小于K的密度,故K与水反应,K不会浮在水面上 | |
| B. | Na2O2具有强氧化性,用途上可用做漂白剂 | |
| C. | Na2CO3俗称“小苏打”,可用于治疗胃酸过多 | |
| D. | K-Na合金因为具有很强的还原性,故可用作原子反应堆的导热剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 晶体中每个Xn+周围有2个等距离且最近的N3- | |
| B. | Xn+中n=l | |
| C. | 该晶体中阳离子与阴离子个数比为3:1 | |
| D. | X元素的原子序数是19 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
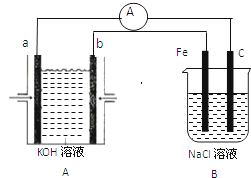 有图所示装置,装置A是氢氧燃料电池,已知该装置工作时电子从b极流向Fe电极.
有图所示装置,装置A是氢氧燃料电池,已知该装置工作时电子从b极流向Fe电极.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com